2. 四川大学 建筑与环境学院,四川 成都 610065;
3. 成都学院,四川 成都 610106
2. College of Architecture & Environment,Sichuan Univ.,Chengdu 610065,China;
3. Chengdu Univ.,Chengdu 610065,China
钛合金比强度高、耐腐蚀性好,是人工关节、人工骨、种植牙等常用硬组织替代物。如何提高植入材料的使用寿命及生物相容性是当下的研究热点。金属植入物材料在人体内的失效主要包括某些合金元素的生理毒性、体内腐蚀与磨蚀、疲劳破坏及骨–人工骨界面的松动等。为了改善骨组织假体界面的骨整合,提高植入物的长期稳定性,对其表面进行生物活性涂层(氧化钛、氮化钛、氧化锆、羟基磷灰石和类金刚石等)处理,是当前采取的主要手段。
金属植入物应用中,除了要考虑组织相容性和耐腐蚀性外,还要考虑生物力学性能,即在保证强度的同时使植入物弹性模量尽量接近骨组织,从而防止因应力遮挡(力学上称为局部应力集中)引起的骨萎缩、骨质疏松和假体松动等。由于纳米晶粒之间存在较大空隙占比,研究表明纳米晶金属材料的弹性模量较母材会有所降低[1]。2004年,卢柯等经过大量实验提出金属表面自纳米化技术,并分析了其机理[2]。从此,掀起了表面自纳米化技术开发和应用研究的热潮。尽管如此,该技术在生物工程领域的研究还不完善,距离临床应用仍需要更多积累。
疲劳裂纹源通常萌生于材料表面或近表面,研究证实表面自纳米化技术可在金属材料内部诱导产生残余压应力和应变硬化[3],产生纳米级微观结构[4],弥合表面微孔[5],从而有效提高材料疲劳性能。对于植入物常用的Ti6Al4V(TC4)钛合金,超声表面冲击技术(Ultrasonic nanocrystal surface modification,UNSM)可以将其108周次时的疲劳强度提高约10%[6],提升幅度虽不及等离子氮化等其他技术[7],但其优点是不改变材料化学成分,表面不产生黑色的异质硬化层(可能带来生物毒性),硬度梯度平缓,表层不会明显脱落。可以预见,随着冲击参数的优化,表面冲击对材料疲劳性能的改善可获得理想的结果,学者们也对UNSM的参数进行了摸索[8–9]。Ferraris等[9]对表面爆炸冲击和再覆膜后TC4的性能进行了研究,认为联合表面处理技术能提升生物力学性能。对于在生理溶液中,晶粒碎化后钛合金的腐蚀性能,由于工艺参数、材料合金元素等的不同[10–11],观察结果并不统一,但其对细胞黏附均有促进作用[12]。有必要对钛合金表面晶粒细化后的相关性能进行深入探索。
为研究超声表面冲击对TC4钛合金生物相容性的影响,对TC4试件进行UNSM处理。利用光学显微镜、电子探针显微分析仪、扫描电子显微镜、超声疲劳试验机、电化学腐蚀方法、X射线能谱分析方法对TC4经UNSM处理后的粗糙度、表面形貌、极化曲线、腐蚀形貌、模拟体液预腐蚀两周后的疲劳性能和断裂特征、纤维软骨细胞的早期黏附等进行分析,揭示UNSM处理后TC4钛合金的生物相容性。
1 试样制备及试验方法实验采用TC4钛合金,其化学成分的质量分数(%)为:C:0.007~0.01,Fe:0.017~0.02,N:0.007~0.009,O:0.190~0.195,H:0.001,Al:6.408~6.411,V:4.403~4.406,其余为Ti。初始试件均为去应力退火(650 ℃下保温4 h)状态。机械性能见表1。材料表面最终经1500#砂纸抛光打磨。
UNSM技术通过压电陶瓷换能器产生频率为20 kHz的激振,从而在试件表面施加每秒几万次的冲击荷载。超声冲击诱使材料表面强塑性变形,导致晶粒细化而生成表层纳米晶。UNSM技术为韩国鲜文大学自主研发,其设备、工艺及理论基础见文献[13]。采用静态荷载为25 N、振幅30 μm、每单位平方毫米冲击36 000次对超声疲劳试件(尺寸见图1)弧中点两侧±5 mm区域进行超声冲击处理。
| 表1 TC4试件的力学性能 Tab. 1 Mechanical properties of TC4 samples |
 |
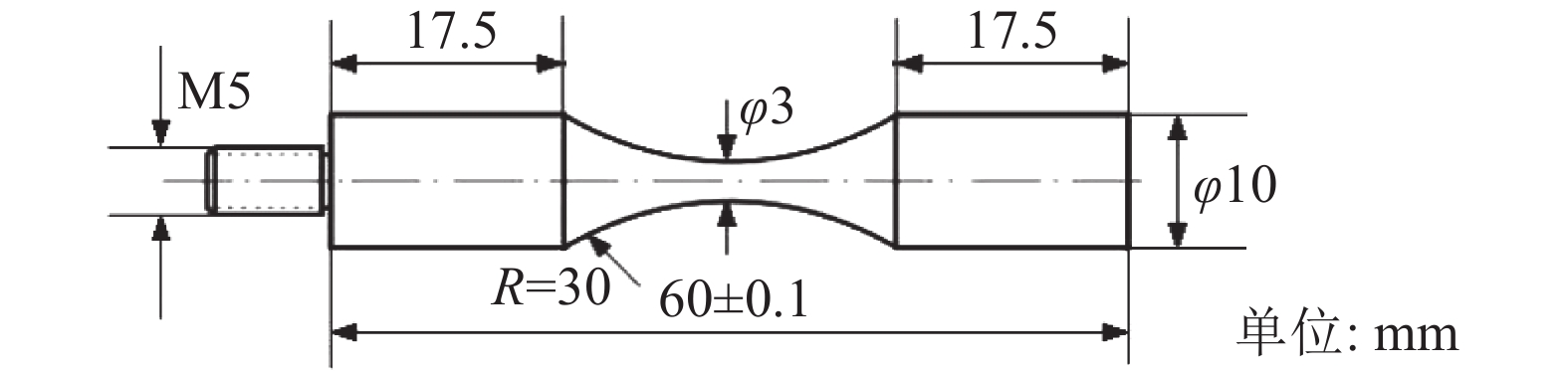 |
| 图1 疲劳试件尺寸 Fig. 1 Dimension of the fatigue specimen |
采用电弧离子镀系统(arc ion plating system,Champion-coating Co.)对对照组TC4试件表面进行复合表面处理(UNSM处理后再镀TiN薄膜),镀膜工艺设置与实际生产中能在TC4表面获得5 μm厚TiN膜的参数一致。
模拟体液根据Kokubo等配方配制[14],恒温37 ℃下,3组TC4试件(未处理、UNSM、UNSM+TiN)在模拟体液中浸泡2周,再进行疲劳试验。电化学腐蚀试验同样以模拟体液作为电解腐蚀液,并采用3极电池,3极分别为铂金、饱和甘汞电极(SCE)和TC4试件,每分钟30 mV进行阳极扫描。试样制备过程为采用环氧树脂+7%乙二胺封样固化24 h以上,腐蚀工作面为超声冲击处理区段的圆柱面,电化学动电位极化曲线测量使用1280腐蚀测量系统完成。
黏附试验所用纤维软骨细胞从小鼠半月板中分离提取,用完全培养基重悬离心管中的细胞,再转入T–25培养瓶中,置于37 ℃、5%CO2的培养箱内进行培养。培养后以合适密度铺入放有钛合金母材(已灭菌,取UNSM冲击段)的96孔板中接种1 h后再进行观察。
使用扫描电子显微镜(Hitachi S–3400N & JEOL JSM–6510LV)对TC4经模拟体液腐蚀后的形貌进行观察。采用ULVAC DEKTAK3接触表面分析仪测量UNSM及混合表面处理后的表面粗糙度。应用岛津USF–2000超声疲劳试验机对UNSM处理前后经模拟体液预浸泡2周的TC4试样进行疲劳试验,频率为20 kHz,应力比为–1。采用JEOL JSM–6510LV型扫描电子显微镜对疲劳断面进行观察,结合X射线能谱分析方法(EDX,JEOL JSM–7500F)对疲劳裂纹源及表面沉积物进行成分分析。利用日立SU8010型扫描电子显微镜对纤维软骨细胞的早期黏附行为进行分析。
2 试验结果与讨论 2.1 超声冲击表面形貌及粗糙度图2比较了未处理、UNSM及复合表面处理试样的表面形貌。
由图2可知:抛光后试样表面留有较细的磨痕;UNSM处理后磨痕变浅,但由于UNSM借助车床操作,随刀具的步进,会在试件表面留下横向规则分布的变形溢出痕迹(两根竖向黑线间距约为80 μm,与步进一致),结合文献[8]中的分析,这种变形溢出与材料表面原始纵向或斜向的微裂纹及初始表面缺陷的交汇处较容易萌生微裂纹,从而导致较高应力水平下的疲劳破坏;超声冲击过的表面再镀TiN薄膜,表面则更为平整。
3组试件的表面平均粗糙度见表2。抛光后,试件平均粗糙度Ra为0.35 μm;超声冲击后,表面粗糙度略有增加达到约0.50 μm(其3维图像见图2(d)),对于植入物材料,适当的粗糙表面有助于细胞黏附,显然UNSM工艺可让TC4表面保持较好的粗糙度;TiN薄膜则有助于改善表面粗糙度。
 |
| 图2 表面形貌 Fig. 2 Surface topography |
| 表2 表面粗糙度 Tab. 2 Surface roughness |
 |
2.2 强塑性变形层
由图3(a)中表层白色散点状α相的流变趋势可得,经UNSM处理后,TC4钛合金获得了约40 μm深的强塑性变形层。利用电子背散射衍射技术绘制出表面与400 μm深(接近母材,仅有微小塑性变形)的极图,由图3(b)、(c)可得,超声表面冲击后,材料表面已获得等轴状且取向随机分布的纳米晶组织。由UNSM处理后TC4的XRD能谱[6],利用文献[15]中去除仪器宽化影响后的修正公式,再由特征峰半峰宽可推得表面晶粒尺寸约60 nm。
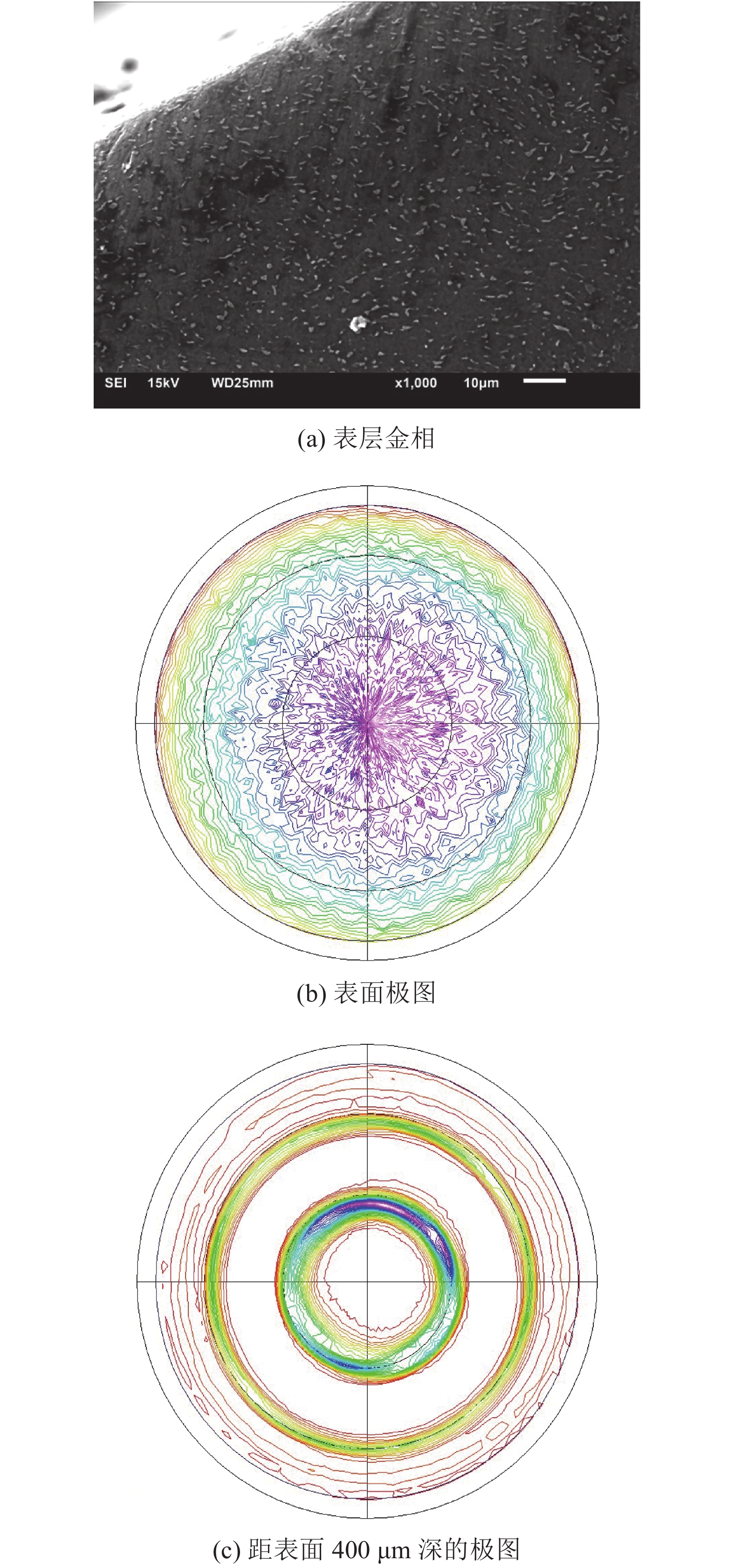 |
| 图3 强塑性变形层观察 Fig. 3 Investigation of SPD layer |
2.3 体液腐蚀形貌、沉积物及极化曲线
模拟体液预浸泡两周后几组TC4试样的腐蚀表面形貌见图4。由图4可知:TC4钛合金抛光后的表面经沉积形成的结节较少,未出现明显点腐蚀,表明TC4钛合金本身具有较好的耐体液腐蚀性;而UNSM处理后,晶粒碎化导致微表面积及表面活性的增加,出现了腐蚀坑,且由UNSM处理过的表面规整,沉积结节与点腐蚀坑散布均匀;复合表面处理试样表面未出现点腐蚀坑,TiN膜的覆盖可有效保护材料表面,且沉积结节在TiN膜上同样均匀分布。
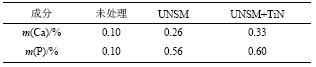
对各试件表面的沉积物结节随机选取6个点分析Ca和P元素的质量百分比再取平均值,结果见表3,表明表面经UNSM处理后可显著增加Ca和P元素的富集,利于种植体进入人体后的融合及康复。
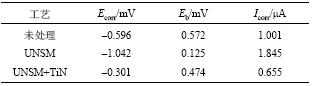
图5中,自腐蚀电位Ecorr为试样在待测溶液中放置10 h以上获得的稳定电位,表4列出了对应的腐蚀数据。在极化曲线测定过程中,由于阴极极化钝化膜被部分还原造成测量中实际的自腐蚀电位下降,即实测的零电流电位;点蚀电位Eb均以电流密度显著上升处为准。在计算自腐蚀电流密度Icorr的过程中,由于阳极极化区难以找到理想的塔菲尔区而不易直接求得,因此本文中的自腐蚀电流密度主要利用阴极极化区计算。由极化曲线可知:UNSM处理后的试样自腐蚀电位Ecorr最低,复合表面处理试样自腐蚀电位最高;UNSM处理后的试样点腐蚀电位Eb最低,而另两组试样的点腐蚀电位接近,表明UNSM处理后表面积或表面活性的增加降低了TC4耐体液腐蚀的性能,而且使TC4试件表面易产生点腐蚀坑,与前文结果一致;自腐蚀电流Icorr反映材料的腐蚀速度,复合表面处理试样的自腐蚀电流最低,表明其耐模拟体液腐蚀的能力最强。综上所述,似乎TC4表面仅UNSM处理会降低TC4钛合金经体液浸泡后的性能。
 |
| 图4 TC4经模拟体液浸泡两周后的表面形貌 Fig. 4 Surface of TC4 after being pre-soaked in SBF for 2 weeks |
| 表3 沉积物中钙磷元素分析 Tab. 3 Analysis of element Ca & P in deposition |
 |
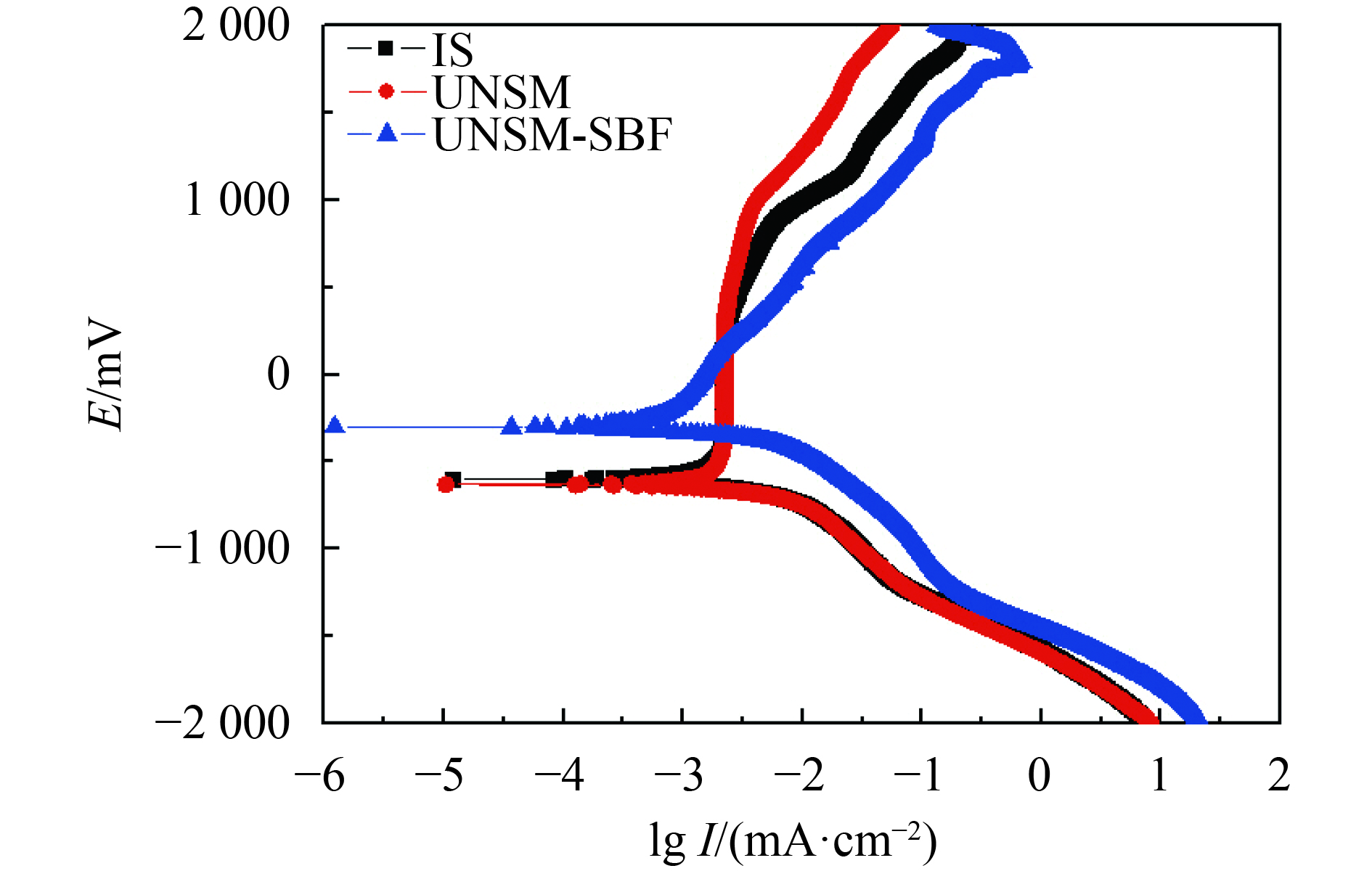 |
| 图5 TC4经模拟体液腐蚀的极化曲线 Fig. 5 Polarisation curves of TC4 in SBF solution |
| 表4 极化曲线特征参数 Tab. 4 Parameters of polarisation curves |
 |
2.4 TC4经模拟体液预浸泡后的疲劳性能
图6给出了TC4经模拟体液预浸泡两周后的疲劳S-N曲线。内部裂纹在图6中用竖线标出。试样疲劳寿命达到108周次以后,若其仍未断裂,则停止疲劳试验,如图6中右箭头所标示。图6表明:UNSM处理后,尽管模拟体液预腐蚀两周后TC4表面出现大量点腐蚀坑,较高的疲劳应力下裂纹主要由表面萌生,但106周次以后裂纹仍大量从内部萌生;材料108周次下的疲劳强度由540 MPa提高到590 MPa;而TiN薄膜较好的耐腐蚀性避免了表面腐蚀坑的生成,进一步将108周次下的疲劳强度提高到约615 MPa,对比文献[6]中的数据,复合表面处理后模拟体液的腐蚀对疲劳强度的影响可忽略(文献[6]中UNSM处理后去应力退火态TC4在108周次下的疲劳强度约为610 MPa,与本文结果基本相当)。
图7(a)和8分别为UNSM组和UNSM-TiN组在模拟体液中浸泡两周后内部起裂试样的裂纹源。UNSM组试件裂纹近表面处可观察到黑色腐蚀产物(图7(a)),EDX分析结果表明,含有模拟体液中的Cl元素及Na元素等(图7(b)),复合表面处理试件则未观察到明显腐蚀产物(图8)。将图7和8与文献[6]中裂纹内部萌生的断面进行比较,鱼眼型裂纹仍然萌生于100~250 μm深的粗晶变形层内,因为该粗晶变形层内残余压应力迅速减小,硬度趋近母材,塑性和韧性较表面强塑性变形层低。模拟体液浸泡两周后的表面点腐蚀坑对裂纹源区的微裂纹向试样表面扩展有影响,但作用较弱,起决定因素的主要是变形后的富α相 (裂纹源核心处亮白色区域)。
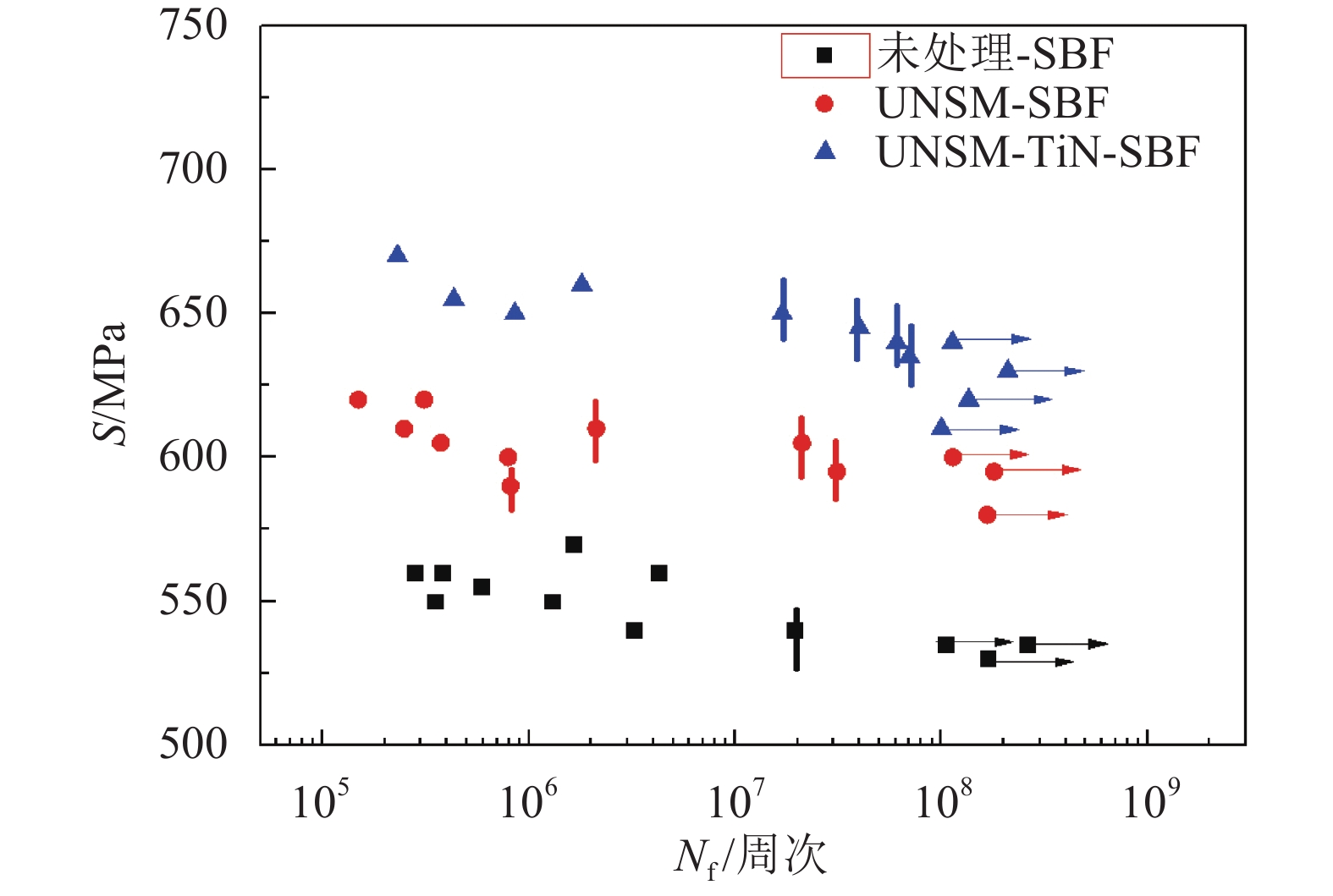 |
| 图6 TC4试样经SBF预浸两周后的疲劳S-N曲线 Fig. 6 S-N curves of TC4 samples which were presoaked in SBF for two weeks |
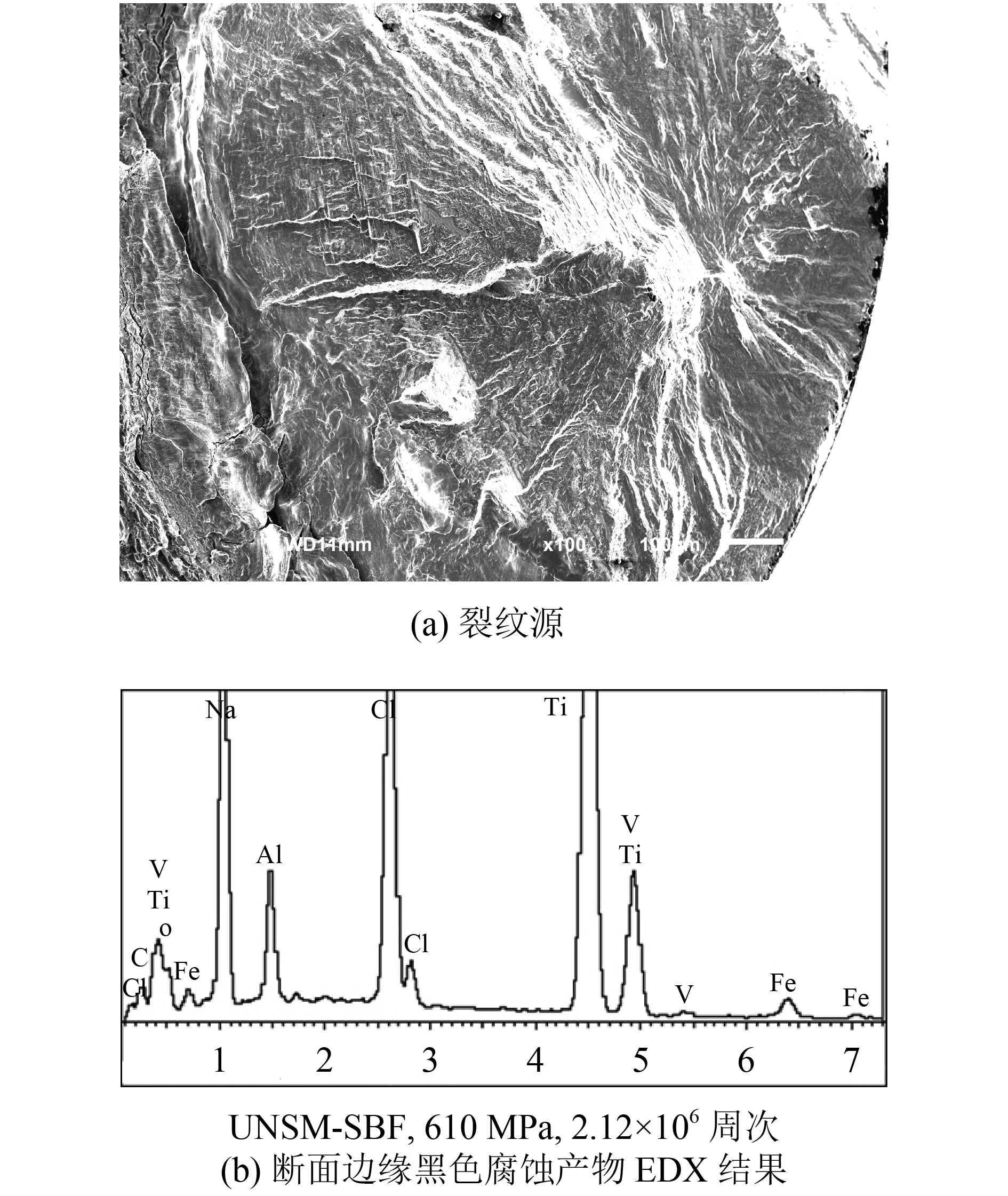 |
| 图7 TC4断面的EDX图 Fig. 7 EDX of fracture surface of TC4 |
 |
| 图8 TC4断面SEM图 Fig. 8 SEM of fracture surface of TC4 |
根据村上公式[16],计算鱼眼型裂纹的应力强度因子,将裂纹源变形α相用椭圆近似,得表面超声冲击后
| ${r_{\rm p}} = \frac{{{{(1 - 2\mu )}^2}}}{\text{π} }{\left( {\frac{{\Delta K}}{{{\sigma _y}}}} \right)^2} \approx \frac{1}{{6\text{π} }}{\left( {\frac{{\Delta K}}{{{\sigma _{\rm y}}}}} \right)^2}$ | (1) |
式中,
由图9可看出:未处理的光滑TC4试件(最后抛光为1500#砂纸)表面细胞外形干瘪,发育较差;表面UNSM处理后,培养1 h后细胞呈球形,外形饱满,纤维丝开始伸展;复合表面处理后,纤维软骨细胞发育最好,纤维丝完全铺开,与种植体融合较好。由以上对比可见:UNSM可促进纤维软骨细胞在种植体表面的早期黏附,纤维丝与超声冲击表面形成紧密的连锁穿插,有利于提高细胞抗剪切力的作用,防止细胞脱落;复合表面经冲击处理后,复合表面形成微孔,微孔表面又会形成微晶,从而使纳米TC4表面的表面能及亲水性提高[17–18],表面积和表面能的提高会促进细胞的早期黏附及矿化沉积,也更易吸附纤维连接蛋白、玻璃体结合蛋白在内的细胞外基质蛋白。玻璃体结合蛋白可进一步促进细胞增殖。
 |
| 图9 TC4表面接种纤维软骨细胞1 h后的形貌 Fig. 9 Observation of fibrochondrocyte after being inoculated on TC4 for 1 h |
3 结 论
1)表面超声冲击后,因为晶粒碎化导致的微表面积增加及表面能的增加,TC4在模拟体液中易产生点腐蚀坑。
2)UNSM处理可促进TC4表面钙磷元素的矿化沉积,利于种植体与受体的融合。
3)表面超声冲击处理后,模拟体液浸泡两周后TC4试样108周次的疲劳强度从540 MPa被提高到约590 MPa。
4)模拟体液预浸两周后,经UNSM处理过的TC4试样均表现为内部萌生裂纹,超声冲击下变形的α相是主要原因。
5)超声冲击后,TC4仍可保持较好的粗糙度,UNSM工艺有助于纤维软骨细胞在TC4表面的早期黏附。
6)UNSM处理后再覆TiN膜,TC4能完全抵御模拟体液浸泡腐蚀对材料疲劳性能的影响,且可获得最好的生物相容性和疲劳性能。
| [1] |
Shen T D, Koch C C, Tsui T Y. On the elastic moduli of nanocrystalline Fe,Cu,Ni,and Cu-Ni alloys prepared by mechanical milling/alloying[J]. Journal of Materials Research, 1995, 10(11): 2892-2896. DOI:10.1557/JMR.1995.2892 |
| [2] |
Lu K, Lu J. Nanostructured surface layer on metallic materials induced by surface mechanical attrition treatment[J]. Materials Science & Engineering A, 2004, 375/376/377(1): 38-45. |
| [3] |
Maawad E, Sano Y, Wagner L. Investigation of laser shock peening effects on residual stress state and fatigue performance of titanium alloys[J]. Materials Science & Engineering A, 2012, 536(1): 82-91. |
| [4] |
Wang T, Wang D P, Liu G. Investigations on the nanocrystallization of 40Cr using ultrasonic surface rolling processing[J]. Applied Surface Science, 2008, 255(5): 1824-1829. DOI:10.1016/j.apsusc.2008.06.034 |
| [5] |
Dekhtyar A I, Mordyuk B N, Savvakin D G. Enhanced fatigue behavior of powder metallurgy Ti-6Al-4V alloy by applying ultrasonic impact treatment[J]. Materials Science & Engineering A, 2015, 641: 348-359. |
| [6] |
Cao Xiaojian, Pyun Youngchik, Jin Jiang. Effect of ultrasonic impact modification on tension-compression fatigue behavior of TC4[J]. China Surface Engineering, 2017, 30(2): 1-8. [曹小建, 片英植, 金江. 超声冲击对TC4钛合金拉压疲劳性能的影响[J]. 中国表面工程, 2017, 30(2): 1-8. DOI:10.11933/j.issn.1007-9289.20170106003] |
| [7] |
Cao Xiaojian, Jin Jiang, Xu Xiaoli. Time duration effect of plasma nitriding on fatigue behavior of S45C steel[J]. Journal of Sichuan University (Engineering Science Edition), 2014, 46(2): 192-197. [曹小建, 金江, 徐小丽. 等离子氮化保温时间对S45C钢疲劳性能的影响[J]. 四川大学学报(工程科学版), 2014, 46(2): 192-197.] |
| [8] |
Cao X J, Murakami R, Pyun Y S. Fatigue properties of a S45C steel subjected to ultrasonic nanocrystal surface modification[J]. Applied Surface Science, 2010, 256(2): 6297-6303. |
| [9] |
Ferraris S, Spriano S, Pan A. Surface modification of Ti-6Al-4V alloy for biomineralization and specific biological response:Part I,inorganic modification[J]. Journal of Materials Science(Materials in Medicine), 2011, 22(3): 533-545. |
| [10] |
Li J, Li S J, Huang H H. Electrochemical and surface analyses of nanostructured Ti–24Nb–4Zr–8Sn alloys in simulated body solution[J]. Acta Biomaterialia, 2014, 10(6): 2866-2875. DOI:10.1016/j.actbio.2014.02.032 |
| [11] |
Wen M, Wen C, Hodgson P. Improvement of the biomedical properties of titanium using SMAT and thermal oxidation[J]. Colloids and Surfaces B:Biointerfaces, 2014, 116(1): 658-665. |
| [12] |
Huang R, Zhuang H Y, Han Y. Second-phase-dependent grain refinement in Ti-25Nb-3Mo-3Zr-2Sn alloy and its enhanced osteoblast response[J]. Materials Science & Engineering C, 2014, 35(3): 144-152. |
| [13] |
Suh M S, Pyun Y S, Suh C M. Variation of fatigue properties in nanoskinned Ti-6Al-4V-rotating bending and axial loading tension-compression cycle[J]. Transactions of the Korean Society of Mechanical Engineers A, 2012, 36(4): 443-449. DOI:10.3795/KSME-A.2012.36.4.443 |
| [14] |
Kokubo T, Takadama H. How useful is SBF in predicting in vivo bone bioactivity[J]. Biomaterials, 2006, 27(15): 2907-2915. DOI:10.1016/j.biomaterials.2006.01.017 |
| [15] |
Feng Gan, Shi Lianjie, Lu Jian. Investigation of surface nanocrystallization of a low carbon steel induced by ultrasonic shot peening[J]. Acta Metallurgica Sinica, 2000, 36(3): 300-303. [冯淦, 石连捷, 吕坚. 低碳钢超声喷丸表面纳米化的研究[J]. 金属学报, 2000, 36(3): 300-303.] |
| [16] |
Liu X H, Sun C Q, Hong Y S. Effects of stress ratio on high-cycle and very-high-cycle fatigue behavior of a Ti-6Al-4V alloy[J]. Materials Science & Engineering A, 2015, 622: 228-235. |
| [17] |
Hejazi I, Seyfi J, Hejazi E. Investigating the role of surface micro/nano structure in cell adhesion behavior of superhydrophobic polypropylene/nanosilica surface[J]. Collids & Surfaces B:Bionterfaces, 2015, 127: 233-240. |
| [18] |
Truong V K, Lapovok R, Estrin Y S. The influence of nano-scale surface roughness on bacterial adhension to ultrafine-grained titanium[J]. Biomaterials, 2010, 31(13): 3674-3683. DOI:10.1016/j.biomaterials.2010.01.071 |
 2018, Vol. 50
2018, Vol. 50


