水性聚氨酯(WPUs)以水作为分散介质,无毒、无气味、无污染,具有绿色环保的特性。由于人们环保意识逐渐增强,WPUs成为聚氨酯工业发展的必然趋势。然而,在WPUs的制备过程中,需引入亲水性离子基团或链段,导致乳胶膜的疏水性能变差,从而使其应用范围受到限制。通过引入低表面自由能的物质,可克服WPUs乳胶膜疏水性能较差的缺点。有机氟化合物具有较低表面自由能,将其引入WPUs体系,含氟链段在WPUs乳胶膜表面富集,可显著提高其乳胶膜的疏水性能。
通常,氟改性水性聚氨酯有两种方式,一种是含氟链段作为主链引入聚氨酯链段中[1–3],另一种是含氟链段以侧链的形式悬挂在聚氨酯主链上。含氟链段作为主链引入聚氨酯,含氟链段的运动受到整个主链的限制,导致含氟链段向表面迁移能力变差,不能显著提高聚氨酯乳胶膜的疏水性能。含氟链段作为侧链悬挂在聚氨酯主链上,只有一端链接在聚氨酯主链上,另一端可自由活动,含氟链段具有较强迁移能力,材料表现出优异的氟表面富集性能[4–7],表面自由能显著降低,疏水性能大幅度提高。目前,含氟链段作为侧链引入聚氨酯,以含氟链段集中分布在聚氨酯端链中的方法为主,该法使聚氨酯的结晶度或分子量变小,导致乳胶膜的力学性能降低[8–9]。因此,在不降低乳胶膜力学性能的前提下,得到具有优异疏水性能的水性含氟聚氨酯(WFPUs)材料成为了亟待解决的问题。
为了提高WFPUs乳胶膜的疏水性能,同时维持其优异的力学性能,并研究含氟侧链长度对WFPUs乳胶膜性能的影响,作者首先合成含氟侧链长度不同的端羟基含氟聚丙烯酸酯:P3FMA、P6FMA和P12FMA,并进一步将含氟链段作为侧链引入WPUs分子链中,含氟侧链沿WFPUs主链分布,得到侧链型WFPUs。采用1HNMR表征了P3FMA、P6FMA和P12FMA的结构。并且通过静态接触角测试及表面自由能计算、XPS、XRD、力学性能测试讨论了含氟侧链长度对WFPUs乳胶膜表面自由能、表面元素组成、结晶度、力学性能的影响。
1 实验部分 1.1 实验原料4, 4'–偶氮双(4–氰基戊醇)(ACP),上海阿拉丁生化科技股份有限公司,分析纯;甲基丙烯酸三氟乙酯(THEMA)、甲基丙烯酸六氟丁酯(HFBMA)、甲基丙烯酸十二氟庚酯(DFHMA),哈尔宾雪佳氟硅化学有限公司,分析纯;正己烷、四氢呋喃,成都市科龙化学试剂厂,分析纯;巯基乙醇(ME),上海麦克林生化科技有限公司,分析纯,使用前不做任何处理;异佛尔酮二异氰酸酯(IPDI):烟台万华聚氨酯股份有限公司;聚丙二醇2 000(PPG,Mn=2 000),龙之族(中国)有限公司;1, 4-丁二醇(BDO)、二羟甲基丙酸(DMPA)、丙酮(AC)、三乙胺(TEA),均为化学纯,成都科龙化工试剂厂;二月桂酸二丁基锡(DBTDL),化学纯,天津市福晨化学试剂厂。
1.2 端羟基含氟聚丙烯酸酯的合成称取适量含氟丙烯酸酯单体溶于四氢呋喃,加入巯基乙醇(ME)和4, 4'–偶氮双(4–氰基戊醇)(ACP),升温到70 ℃,反应15 h。反应完成后,减压蒸馏除去大部分四氢呋喃溶剂,然后将含有聚合物的溶液滴加到大量正己烷中,放入冰箱过夜,再用正己烷洗涤聚合物3~5次,除去小分子和未反应的单体,将该聚合物在40~60 ℃下真空干燥24 h左右,得到数均分子量大小在2 100~3 600之间的端羟基含氟聚丙烯酸酯P3FMA、P6FMA和P12FMA。其合成路线见图1,具体配方见表1。
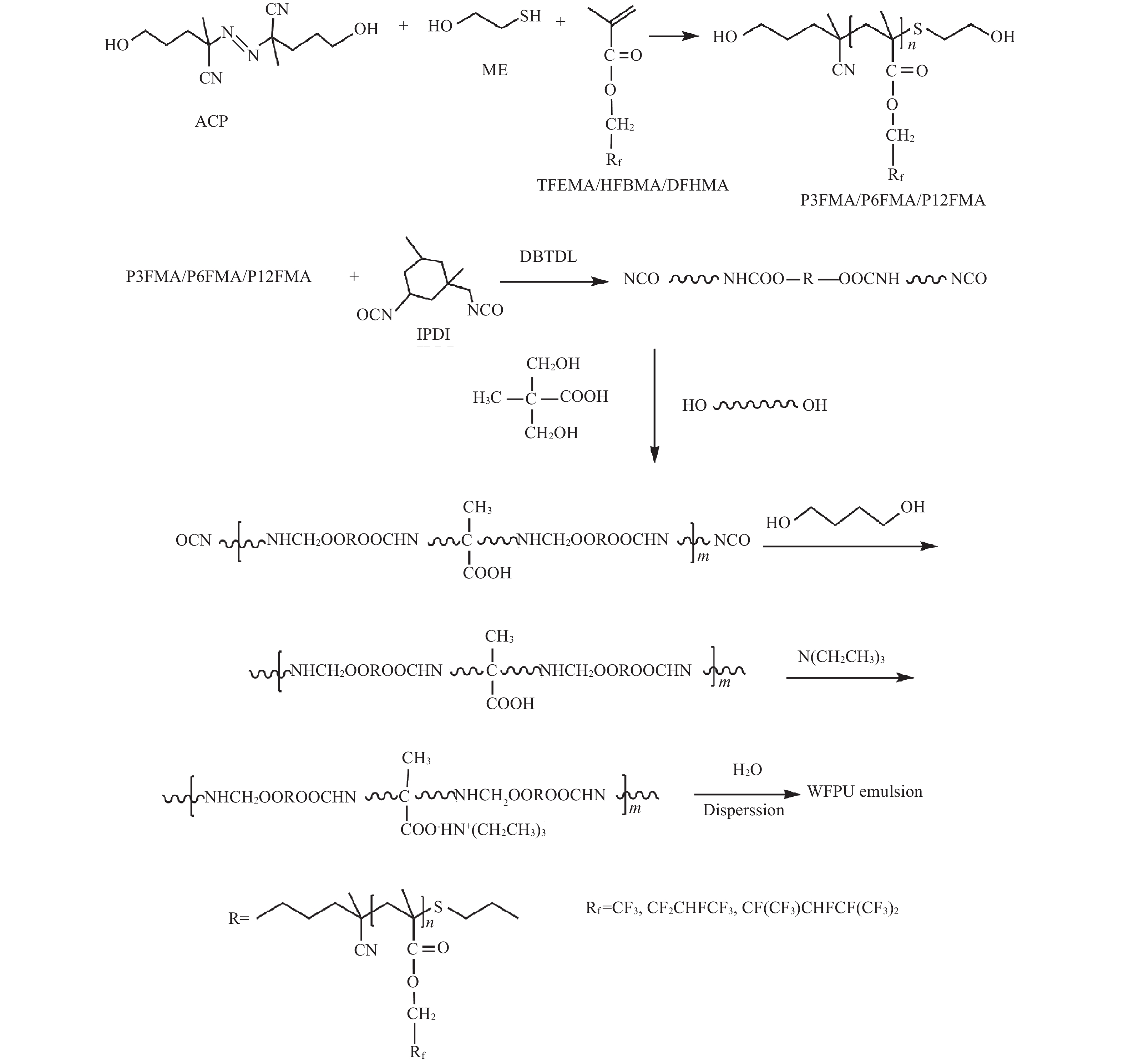 |
| 图1 端羟基含氟聚丙烯酸酯及水性含氟聚氨酯的合成路线 Fig. 1 Synthesis of by hydroxyl–terminated poly (fluoroalkyl methacrylates) and waterborne fluorinated polyurethane |
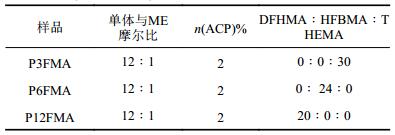
| 表1 端羟基含氟聚丙烯酸酯的配方 Tab. 1 Recipes of hydroxyl–terminated poly (fluoroalkyl methacrylates) |
 |
1.3 端羟基含氟聚丙烯酸酯改性水性聚氨酯的合成
将端羟基含氟聚丙烯酸酯溶于丙酮,与IPDI一起加入反应器。在85 ℃,DBTDL作用下反应3 h,得到异氰酸根封端的含氟低聚物。然后加入真空脱水处理的PPG和5 g DMPA,在85 ℃下继续反应3 h,降温至70 ℃,加入扩链剂BDO,反应到异氰酸根含量到达理论值。降温到35 ℃,加入中和剂TEA中和30 min,最后在高速搅拌下加入去离子水分散扩链,得到WFPUs乳液。分采用P3FMA(0.15 0.46、0.76、1.07、1.53、3.06、4.59 g)、P6FMA(0.11、0.34、0.57、0.80、1.14、2.28、3.42 g)和P12FMA(0.09、0.27、0.45、0.64、0.91、1.82、2.73 g)改性WPUs,通过调节氟含量,得到3个系列的WFPUs,分别命名为WFPUs–P3FMA、WFPUs–P6FMA、WFPUs–P12FMA。按照上述方法制备WPU为参照样。WPU及WFPUs的合成路线见图1,合成配方见表2。
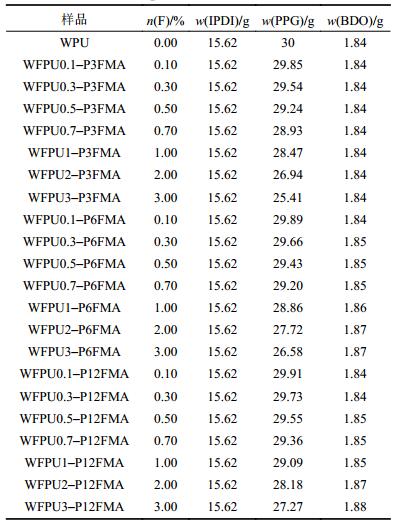
| 表2 WPU及WFPUs的原料配方 Tab. 2 Composition of WPU and WFPUs |
 |
1.4 乳胶膜的制备
将乳液均匀地铺展在聚四氟乙烯板上,在室温下干燥3 d,得到乳胶膜。然后将上述乳胶膜放入真空烘箱,60 ℃下干燥24 h,除去所有水分。最后,得到厚度约为0.50 mm的乳胶膜并保存在干燥器中备用。
1.5 1HNMR实验1HNMR谱由Bruker AC600(600 MHz)型核磁共振仪测定,采用氘代丙酮为溶剂,四甲基硅烷(TMS)为内标。
1.6 FTIR实验采用Nicolet 560 型红外光谱分析仪测试样品的红外光图谱。每个样品在650~4 000 cm–1范围内扫描32次,分辨率是为4 cm–1。
1.7 乳胶膜的静态接触角测定和表面自由能计算乳液在干净的载玻片上成膜自然干燥后,在120 ℃下烘6~8 h。在干燥器中放置1 d,用DSA–25S型接触角测试仪测试乳胶膜的静态接触角。取液滴与玻璃片接触25 s时的接触角为稳定接触角,每个样品测定7次,取平均值为最终接触角。并采用Owens–Wendt法[10]计算表面自由能,如式(1)所示:
| $\left\{\begin{aligned} & {\gamma _{\rm L1}}(1 + \cos \; {\theta _1}) = 2{({\gamma_{\rm L1}^{\rm d}}{\gamma_{\rm s} ^{\rm d}})^{1/2}} + 2{({\gamma _{\rm L1}^{\rm p}}\gamma _{\rm s}^{\rm P})^{1/2}},\\ & {\gamma _{\rm L2}}(1 + \cos \; {\theta _2}) = 2{({\gamma_{\rm L2}^{\rm d}}{\gamma_{\rm s} ^{\rm d}})^{1/2}} + 2{({\gamma _{\rm L2}^{\rm p}}\gamma _{\rm s}^{\rm P})^{1/2}} \end{aligned}\right. $ | (1) |
式中,
采用XSAM 800型X光电子能谱仪(XPS,Al靶单色化的X光源)测试乳胶膜距表层10 nm的元素组成。
1.9 乳胶膜的XRD分析采用X’pro MPD DY129型X射线衍射仪测定薄膜的结晶性能。入射光源为CuKα(λ=0.154 1 nm),测试电压为35 kV,电流为30 mA,扫描范围为5°~50°。乳胶膜的厚度为0.50 mm。
1.10 乳胶膜力学性能的测定采用4302型拉伸仪(美国,instron)测试乳胶膜的力学性能。拉伸速率为100 mm/min,测试温度为25 ℃。测试样品为哑铃状,中间伸展部分长33.0 mm,宽6.0 mm,厚0.5 mm。每个样品测试5次,取平均值作为最终的结果。
2 结果与讨论 2.1 端羟基含氟聚丙烯酸酯的结构表征图2(a)、(b)和(c)分别为P3FMA、P6FMA和P12FMA的1HNMR谱图。2.80和1.90分别为水和氘代丙酮的特征峰。在这3幅图中,5.60左右均没有出现碳碳双键氢原子特征峰,说明含氟丙烯酸酯已反应完全。
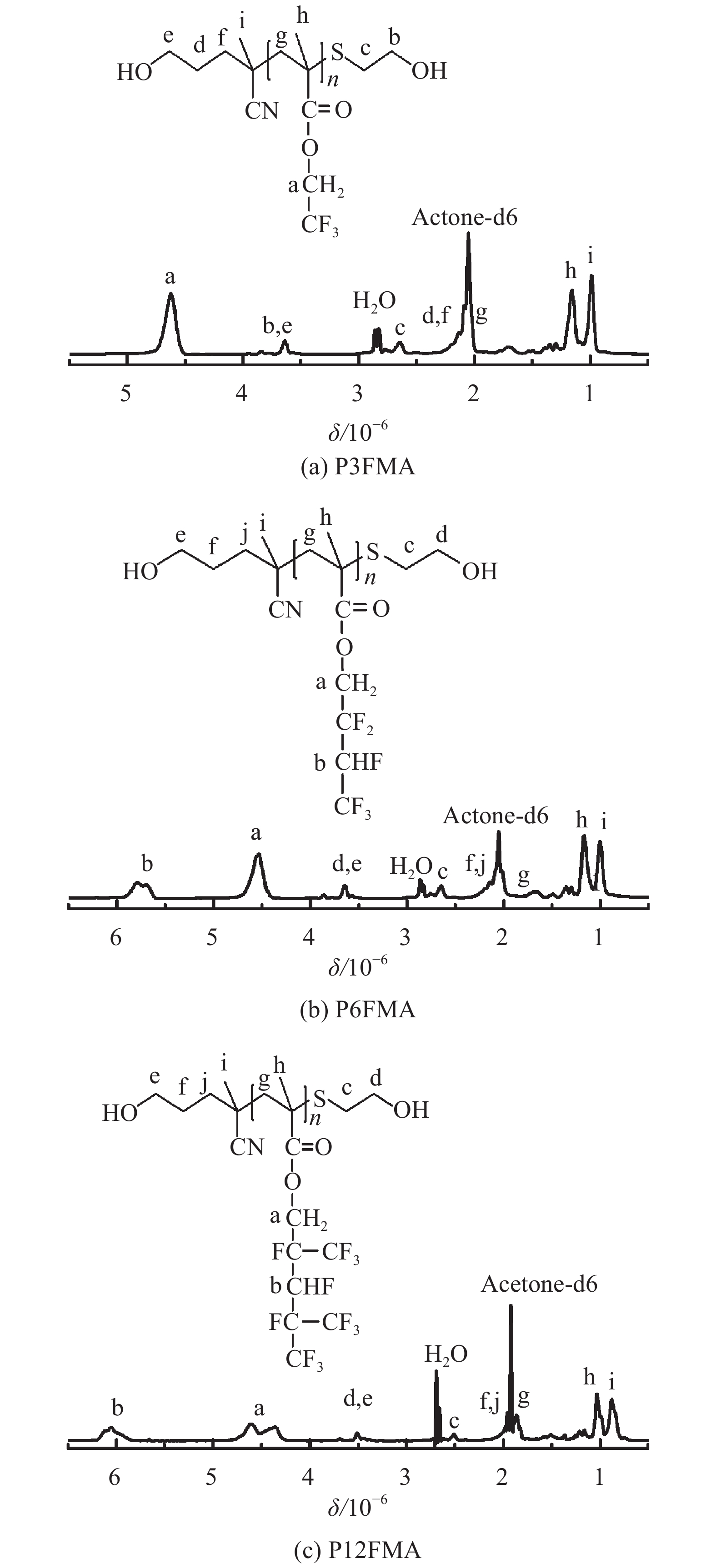 |
| 图2 端羟基含氟聚丙烯酸酯的1HNMR谱图 Fig. 2 1HNMR spectra of hydroxyl–terminated poly (fluoroalkyl methacrylates) |
在图2(a)中,P3FMA侧链中—CH2—基团氢原子化学位移在4.61处,与—OH基团邻近的—CH2—基团氢原子化学位移在3.64处,这说明成功将—OH基团引入了含氟产物。由于S元素的电负性低于O元素的电负性,所以与S元素邻近的—CH2—基团氢原子的化学位移在2.65处。a处氢原子峰的积分面积与c处氢原子峰的积分面积比为11.86∶1,此值与投料中TFEMA与ME的摩尔比12∶1相当。因此通过1H NMR得到的实际值与投料比的理论值接近。以上结果说明成功合成了P3FMA。图2(b)中,5.80左右的特征峰属于—CHF基团氢原子化学位移。4.56是与—COO—基团相连的—CH2—基团氢原子的特征峰。3.64处归属于—CH2—基团(与—OH基团相连)氢原子化学位移。2.65左右的特征峰属于与S元素相连的—CH2—基团氢原子化学位移。a处氢原子的积分面积与c处氢原子的积分面积之比为12.93∶1,与投料中n(HFBMA) ∶ n(ME)=12∶1相当。此结果说明成功合成了端羟基含氟聚丙烯酸酯P6FMA。在图2(c)中,6.15特征峰属于—CHF基团的氢原子化学位移。4.50是侧链中的—CH2—基团氢原子的化学位移。3.52 ppm左右归属于—CH2—基团(与—OH基团相连)氢原子的特征峰,2.50左右属于与S元素相连的—CH2—基团氢原子的特征峰。特征峰a与c的积分面积之比为12.30∶1,此值与投料中n(DFHMA)∶n(ME)=12∶1接近。以上分析说明成功合成了端羟基含氟聚丙烯酸酯P12FMA。
2.2 乳胶膜的红外光谱分析乳胶膜WPU、WFPU2–P3FMA、WFPU2–P6FMA和WFPU2–P12FMA的FTIR图谱显示于图3。从图3可知,所有图谱均显示了氨基甲酸酯的特征峰:3 340 cm–1左右为N—H的伸缩振动峰,1 530 cm–1左右为N—H的弯曲振动峰,1 712 cm–1左右为C=O的伸缩振动峰。以上分析表明成功地合成了WPUs。从图3还可以看出,WFPUs与参照样WPU的差异:3种WFPUs乳胶膜在967 cm–1左右处出现了—CF3的伸缩振动特征吸收峰,在指纹区701、680 cm–1左右出现了—CF3在平面和非平面内摇摆振动相结合的特征吸收峰,而在WPU中却没有观察到这些特征峰。由此说明成功地将含氟链段作为侧链引入了WFPUs分子链中。
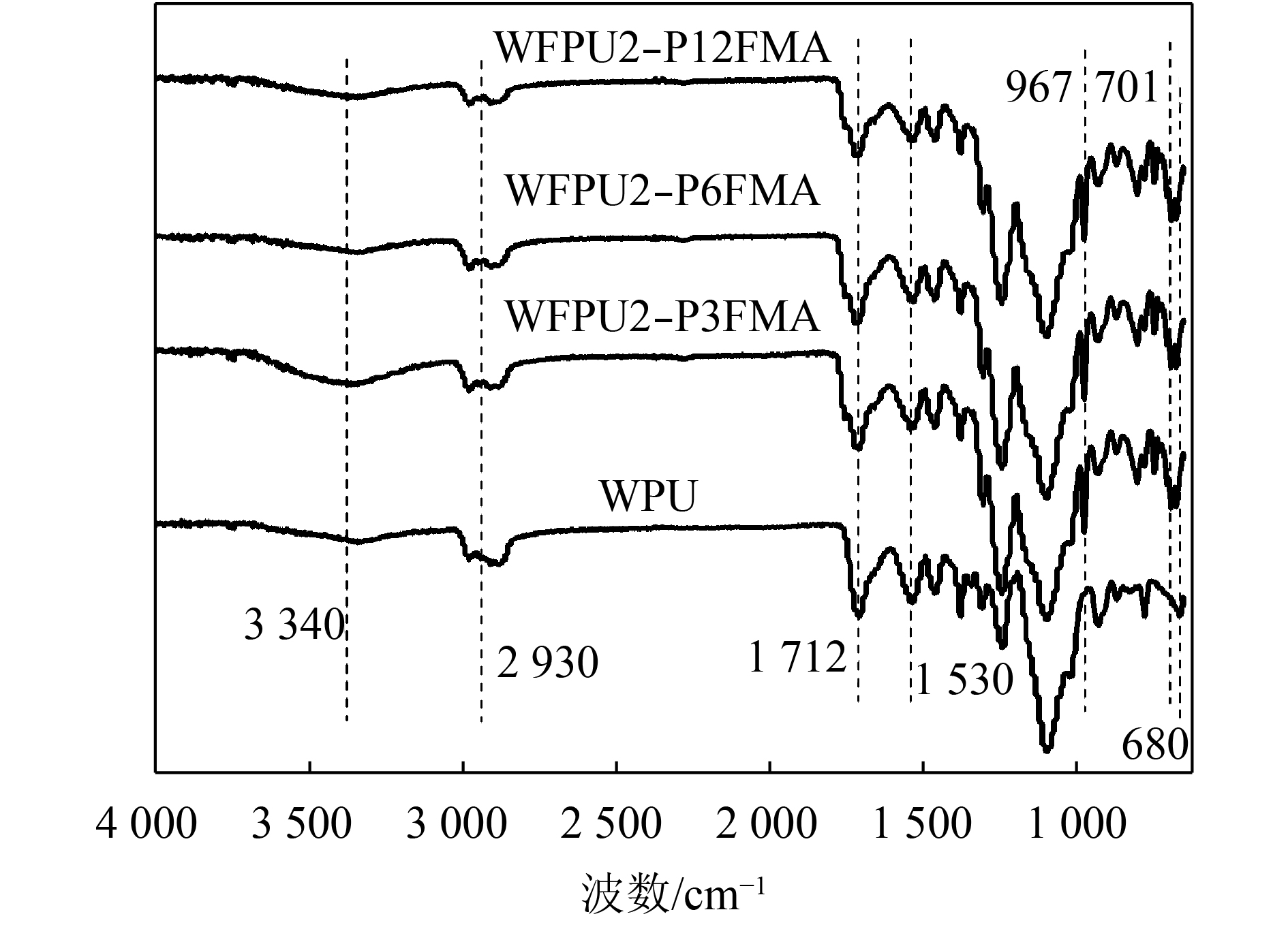 |
| 图3 WPU和WFPUs乳胶膜的FTIR图谱 Fig. 3 FTIR spectra of WPU and WFPUs films |
聚氨酯中的氢键作用可通过对FTIR结果分峰处理来研究[11–14]。聚氨酯的羰基区(C=O)是最适合研究氢键的结构[15],氢键化C=O含量以及氢键的强度代表了硬段与硬段的作用力大小。在本研究中,WFPUs只含有一种氢键供体即硬段中的N—H,氢键受体包括以下3种:硬段中的C=O,软段中的醚键(C—O—C)以及含氟链段中的C—F。采用高斯函数对WPU及WFPUs C=O区进行拟合分峰的结果显示于图4。由图4可知,C=O区出现了3个拟合峰,从左到右依次是:有序氢键化C=O峰,无序氢键化C=O峰和自由C=O峰。3个峰积分面积的百分含量和对应的波数列于表3。
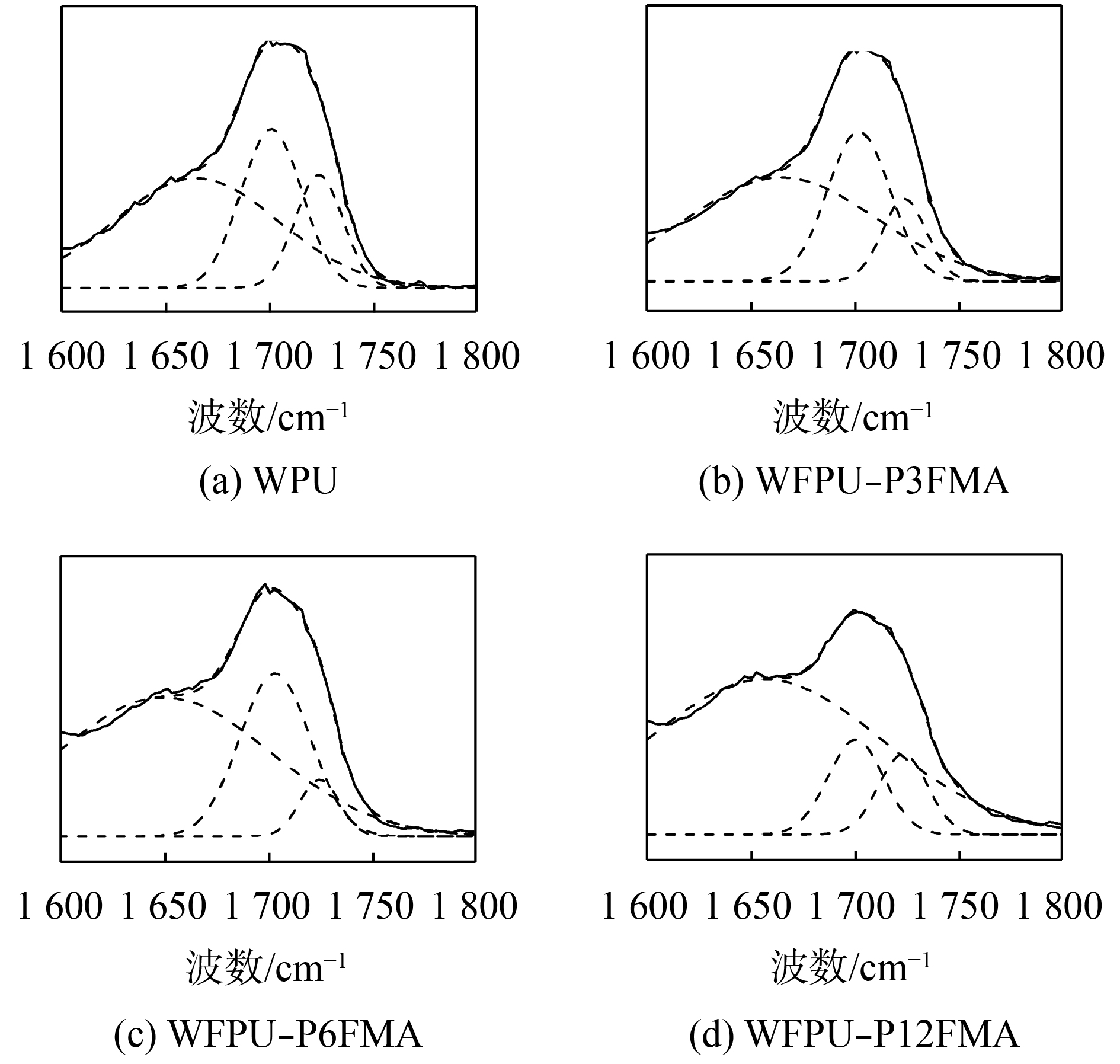 |
| 图4 WPU和WFPUs乳胶膜羰基区分峰结果 Fig. 4 Deconvolution results of WPU and WFPUs films in the carbonyl groups region |
| 表3 WPU和WFPUs乳胶膜羰基区分峰结果数据 Tab. 3 Deconvolution calculated results of the WPU and WFPUs films |
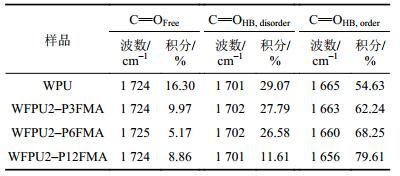 |
从表3可知,将P3FMA、P6FMA和P12FMA引入WPUs后,氟含量均为2%的条件下,随着含氟侧链长度增加,对应WFPUs有序氢键化C=O含量分别升高到62.64%、68.25%和79.61%;而对应的波数分别降低到1 663、1 660和1 656 cm–1,这说明随着含氟侧链长度增加,硬段间的相互作用增加。这可能是因为,含氟侧链越长,端羟基含氟聚丙烯酸酯均聚物的氟含量越高,对C=O的电子云密度影响越大,氢键化C=O含量越高[16–17]。
2.3 乳胶膜的静态接触角和表面自由能通过测试去离子水和二碘甲烷在WFPUs乳胶膜上的静态接触角来研究其疏水性能。WPU、WFPUs–P3FMA、WFPUs–P6FMA和WFPUs–P6FMA乳胶膜对水的静态接触角显示于图5。从图5可知,随着氟含量增加,3个系列的WFPUs乳胶膜对水的静态接触角先急剧增加,然后达到一个平台区(最大静态接触角),随后继续增加氟含量,水静态接触角大小没有明显变化。含氟侧链长度最短的乳胶膜WFPUs–P3FMA达平台区的最低氟含量为2%,对应水静态接触角约为98°;含氟侧链长度居中的乳胶膜WFPUs–P6FMA达平台区的最低氟含量为1%,对应静态接触角约为102°;含氟侧链长度最长的乳胶膜WFPUs–P12FMA达平台区所需最低氟含量仅为0.5%,而对应静态接触角则高达108°。由此可见,3种WFPUs乳胶膜的疏水性能均得到提高,增加含氟侧链长度,不仅可降低含氟乳胶膜达到最大静态接触角所需氟含量,而且可提高其最大静态接触角,乳胶膜表现出更优异的疏水性能。另外,这个结果也说明,含氟侧链的长度决定着含氟乳胶膜所能达到的最大静态接触角和到达最大静态接触角所需的最低氟含量。
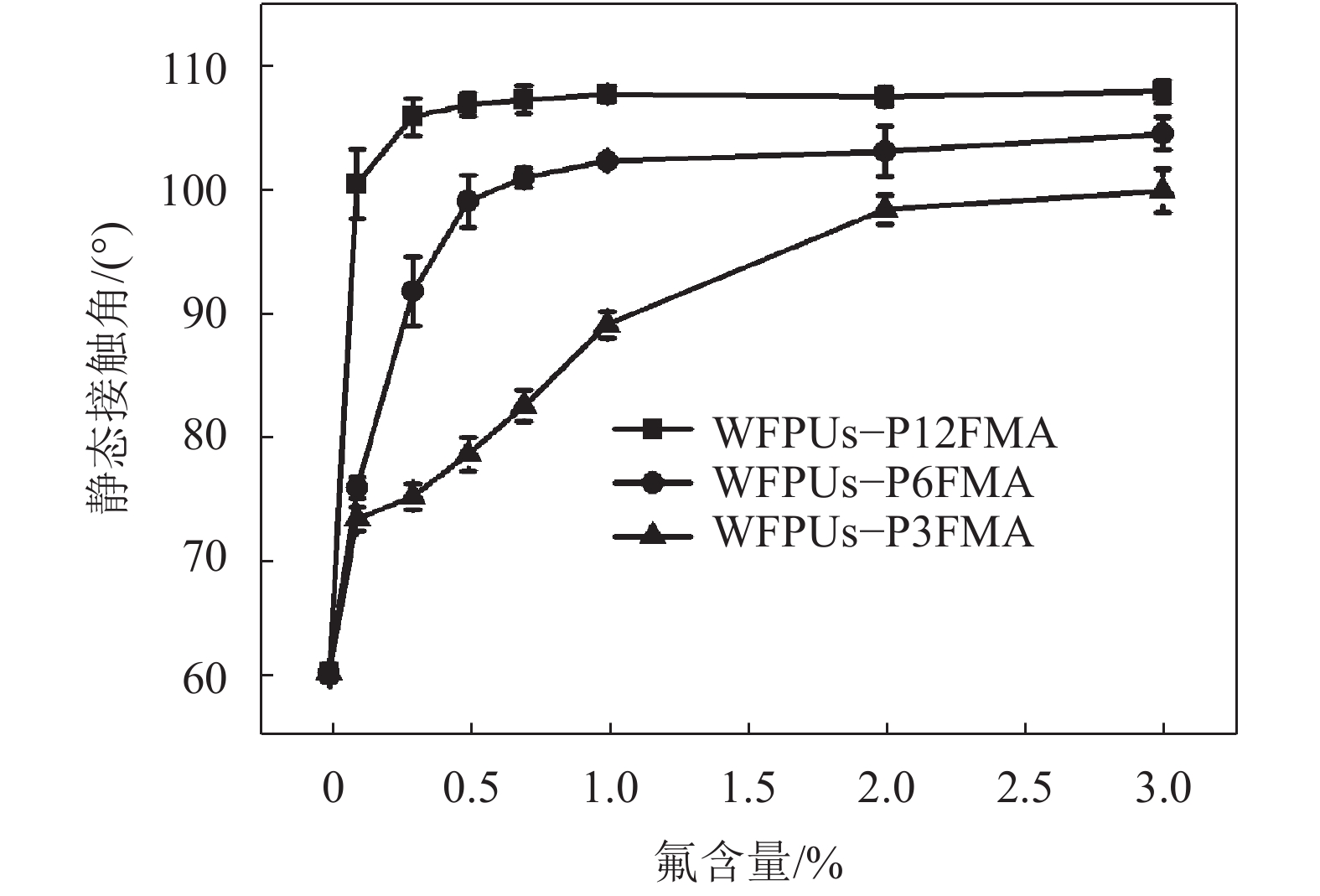 |
| 图5 WPU及WFPUs乳胶膜的水静态接触角 Fig. 5 Water static contact angle of WPU and WFPUs films |
图6显示了二碘甲烷液滴在WPU及WFPUs乳胶膜表面上的静态接触角随氟含量的变化。从图6可知:随着氟含量增加,WFPUs乳胶膜对二碘甲烷的静态接触角的变化趋势与对水的静态接触角的变化趋势类似。WFPUs–P3FMA、WFPUs–P6FMA和WFPUs–P12FMA乳胶膜对二碘甲烷的最大静态接触角分别为49°、55°和83°,达到对应最大静态接触角所需要的最低氟含量分别为2%、1%和0.5%。因此,二碘甲烷和水在乳胶膜表面上达到最大静态接触所需氟含量一致。
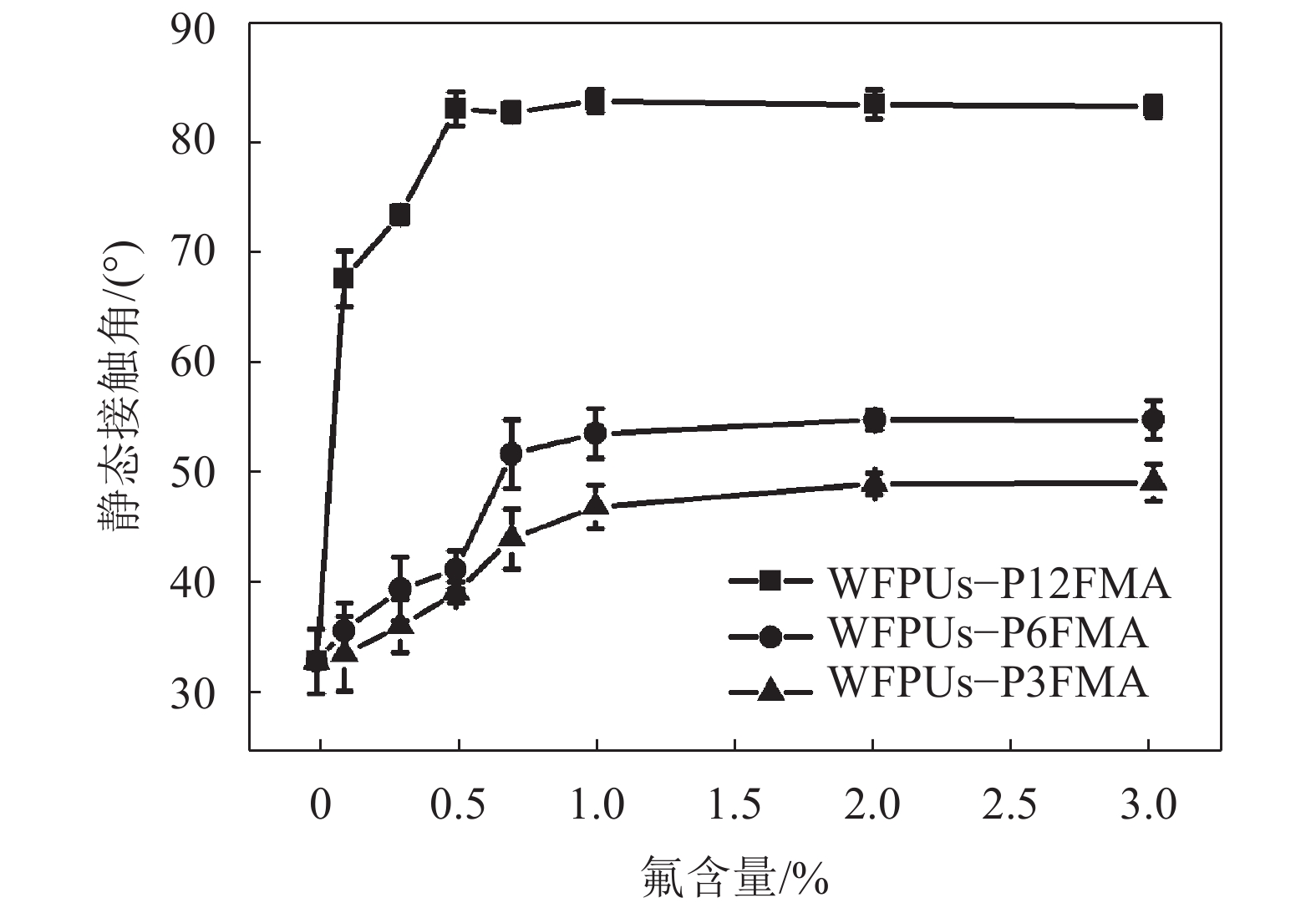 |
| 图6 WPU和WFPUs乳胶膜二碘甲烷静态接触角 Fig. 6 Methylene iodide static contact angle of WPU and WFPUs films |
图7是采用Owens–Wendt法得到的乳胶膜的表面自由能。由图7可知:当氟含量为2%时,含氟侧链最短的乳胶膜WFPUs–P3FMA12的表面自由能达到其最低值34.78 mN/m;当氟含量为1%时,WFPUs–P6FMA乳胶膜的表面自由能达到其最低值32.41 mN/m;当氟含量为0.5%时,含氟侧链最长的乳胶膜WFPUs–P12FMA的最低表面自由能约为15.94 mN/m。
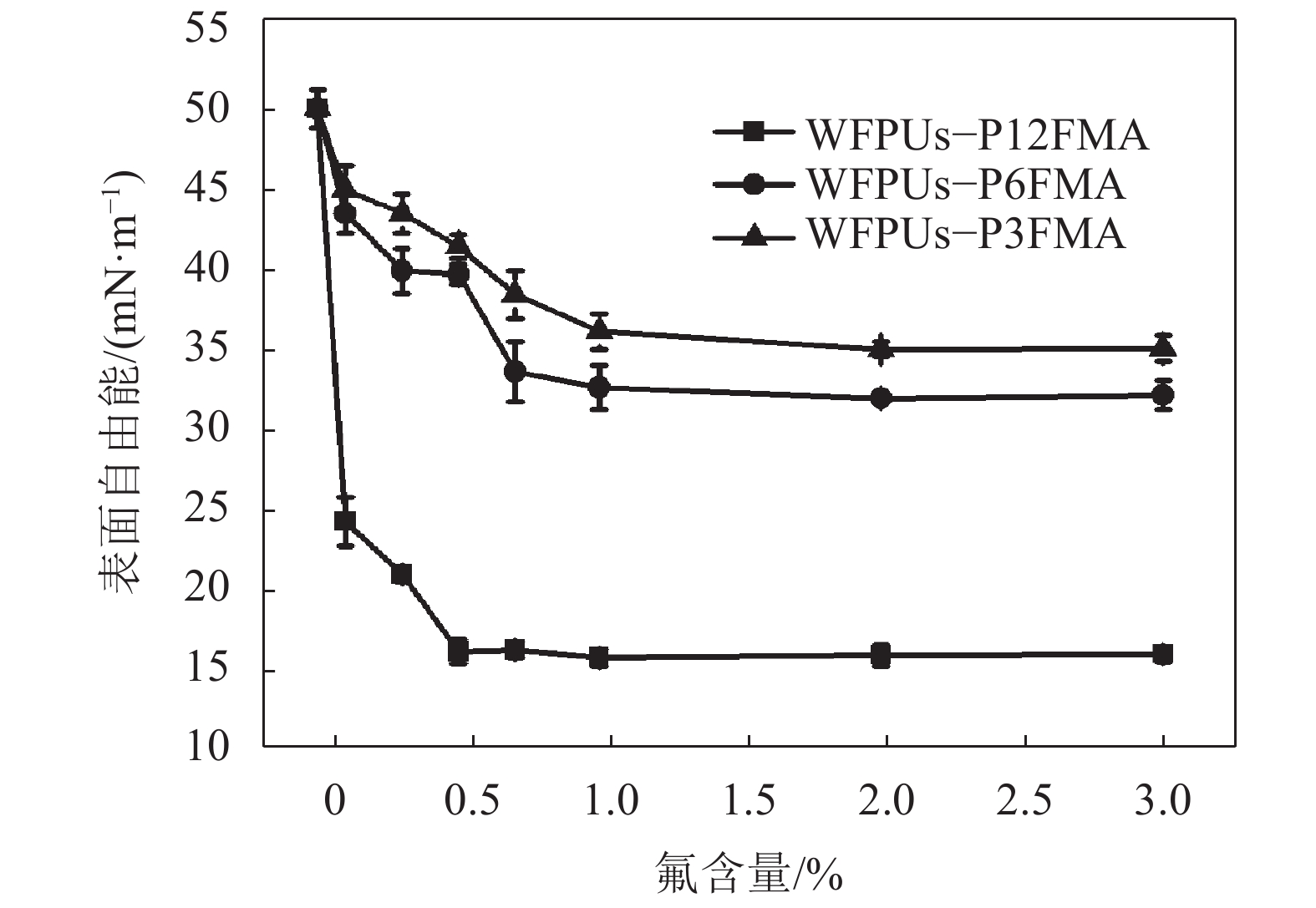 |
| 图7 WPU和WFPUs乳胶膜的表面自由能 Fig. 7 Surface free energy of WPU and WFPUs films |
由此可知,含氟侧链最长的乳胶膜WFPUs–P12FMA的表面自由能最低,甚至低于聚四氟乙烯的表面自由能18 mN/m。因此较长的含氟侧链可更加有效地降低WFPUs乳胶膜的表面自由能,提高其疏水性能。这是因为较长的含氟侧链的迁移性更好,其在表面的富集性更强,因此,会更加有效地降低表面自由能。
2.4 乳胶膜的表面元素组成为了研究含氟侧链向WFPUs乳胶膜表面的迁移富集特征,采用XPS对乳胶膜的表面元素组成进行分析,检测深度距乳胶膜表层为10 nm。图8(a)、(b)和(c)分别显示了WFPUs–P3FMA、WFPUs–P6FMA、WPU及WFPUs–P12FMA乳胶膜表面XPS图谱随氟含量变化。氟含量大于0.5%,所有样品均显示了F、O、N、C信号峰:F(特征结合能在689 eV处的F1s);O(特征结合能在532 eV处的O1s);N(特征结合能在400 eV处的N1s);C(特征结合能在284~294 eV之间的C1s)。
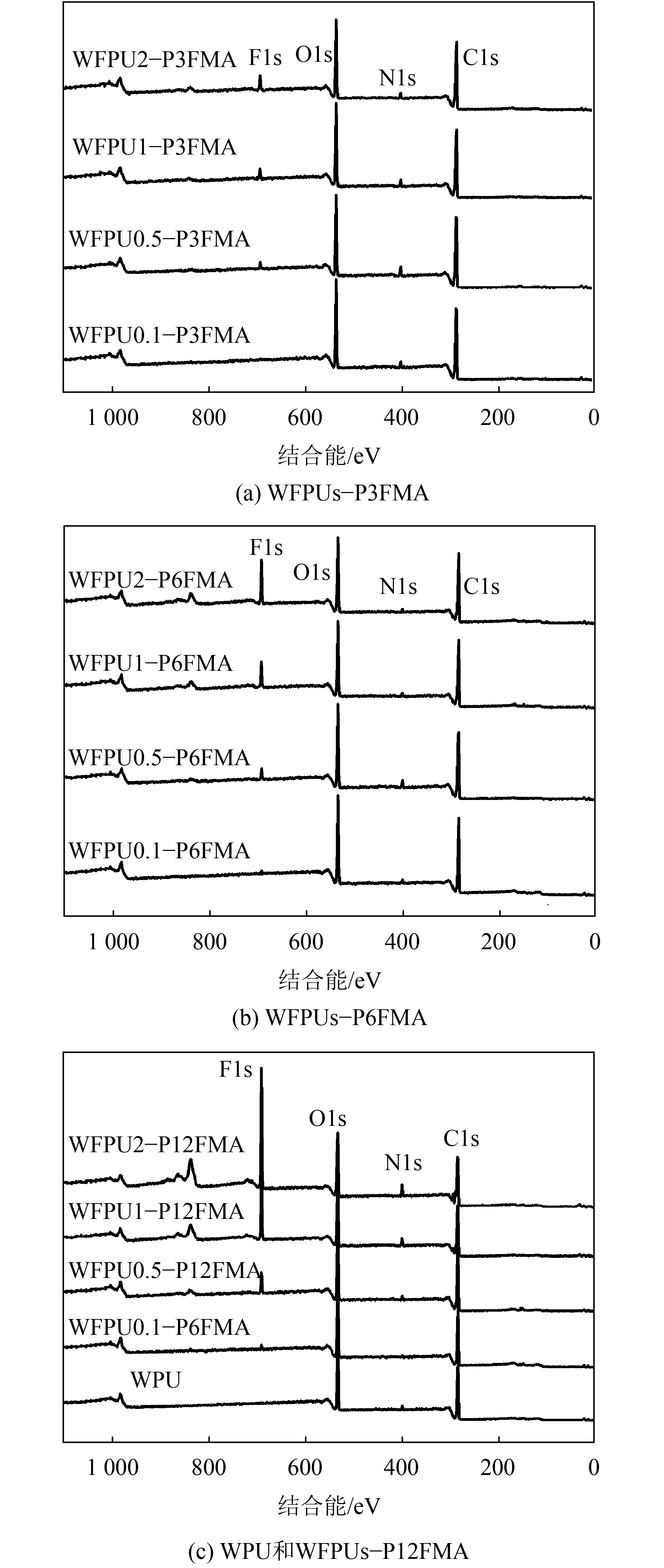 |
| 图8 WPU及WFPUs乳胶膜的XPS谱图 Fig. 8 XPS spectra of the WPU and WFPU films |
表4是根据XPS的灵敏度因子法计算出了F、O、N、C的表面含量[18]。由表4可知,与WPU乳胶膜比较,所有WFPUs乳胶膜表面上都检测到了氟元素,并且表面上的氟含量都大于本体的平均氟含量,这说明含氟侧链发生了表面迁移富集行为。对于3个系列WFPUs乳胶膜,其表面的氟含量都随着本体平均氟含量的增加而增加,这就有效地提高了乳胶膜表面的静态接触角,降低了表面自由能。在本体平均氟含量相同的情况下,随着含氟侧链长度的增加,表面氟含量逐渐增加。WFPUs–P3FMA、WFPUs–P6FMA和WFPUs–P12FMA乳胶膜的氟表面富集因子(FSEF)分别是:2~4、5~7和10~18。这表明WFPUs乳胶膜的氟表面富集因子同样随着含氟侧链长度增加而增加,含氟侧链越长,表面迁移富集性能更好,所以含氟侧链最长的WFPUs–P12FMA乳胶膜的表面自由能最低。
| 表4 WPU及WFPUs乳胶膜表面和本体的元素组成 Tab. 4 Surface and bulk composition of the WPU and WFPUs films |
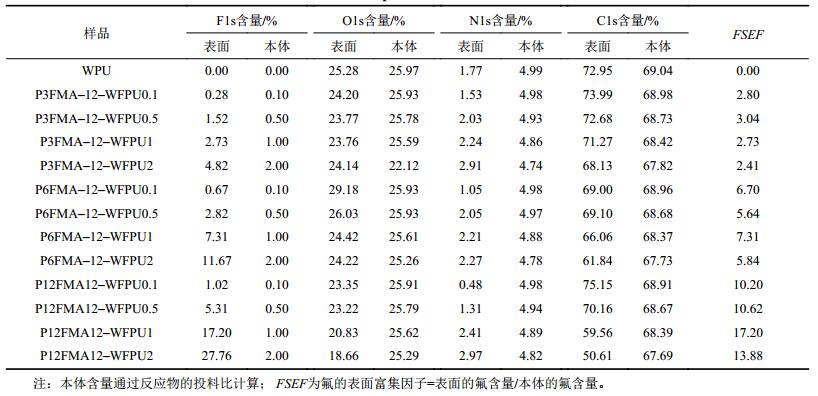 |
另外,从表4还可以看出,对于3个系列WFPUs乳胶膜的氟表面富集因子都随本体中平均氟含量的增加先增加后降低。这表明在较低本体氟含量时,含氟侧链向表面的迁移性更好,而在较高本体氟含量时,含氟侧链向表面的迁移性能降低[19]。
表4显示了氮元素含量随着氟元素含量的增加而增加。这是因为含氟链段中C—F与硬段中N—H之间存在较强的氢键作用,当氟元素向表面迁移的时,由于这种氢键作用的存在,使得氮元素也向表面迁移,所以随着表面氟含量增加,表面氮元素含量也增加。值得指出的是,WFPUs乳胶膜的表面自由能并不是随着表面氟含量的增加而无限地降低。含氟侧链对表面自由能的降低存在一个临界表面含量,当高于这个临界表面含量后,材料的表面自由能将不再随着氟含量增加而降低。材料表面自由能是由表面元素的组成、含氟侧链在表面的定向排列和分布[20]、表面的几何形貌共同决定的。通过添加低表面自由能的材料,只能在一定程度上降低材料的表面自由能。
2.5 乳胶膜的XRD衍射分析WFPUs是一种由软硬段交替组成的嵌段共聚物。在一定条件下,硬段可以聚集在一起,形成结晶微区。XRD曲线上的结晶衍射峰代表了这种材料的结晶微区[21]。WPU和WFPUs乳胶膜的X衍射分析如图9所示。
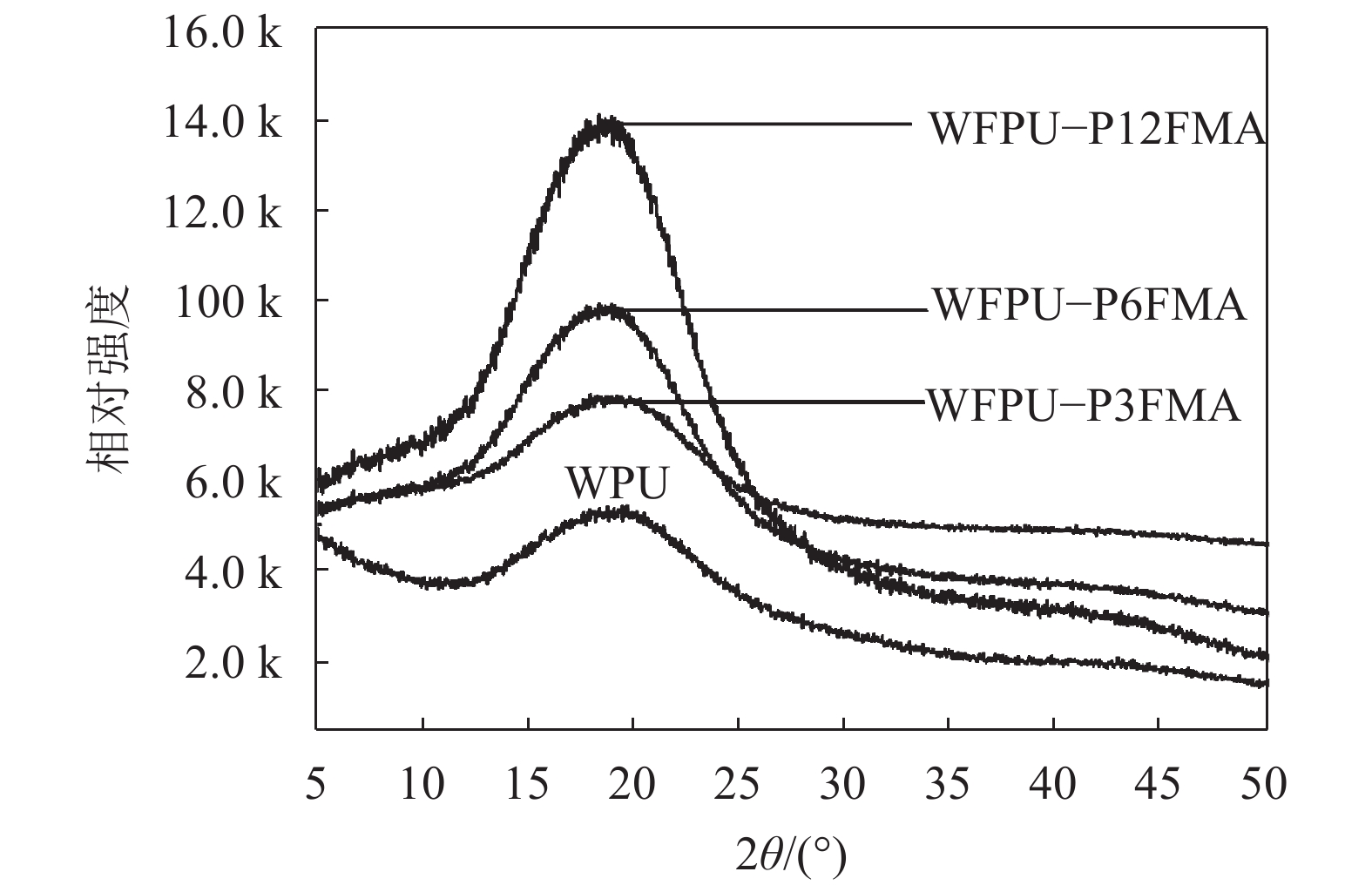 |
| 图9 WPU及WFPUs乳胶膜的XRD图谱 Fig. 9 XRD patterns of the WPU and WFPUs films |
由图9可知:WPU和WFPUs在2θ=19°左右均呈现一个衍射峰,这是由硬段的结晶微区所引起。当氟含量均为2%时,含氟侧链最长的乳胶膜WFPUs–P12FMA在2θ=19°时的衍射峰强度最大。这表明WFPUs乳胶膜的结晶度随着含氟侧链长度的增加而增加。这是因为氢键作用会影响WFPUs硬段的聚集状态,从而影响其结晶度,正如上面FTIR分峰结果所表明,引入含氟侧链后,随含氟侧链长度增加,硬段中有序氢键化C=O的百分含量增加。这种有序结构有利于硬段链段有序排列,其含量的增加使硬段形成更多微晶区,因此,结晶度随着含氟侧链长度增加而增加。
2.6 乳胶膜的力学性能聚氨酯的力学性能与其实际应用密切相关。表5列出了WPU、WFPUs–P3FMA、WFPUs–P6FMA和WFPUs–P12FMA乳胶膜力学性能测试结果。
| 表5 WPU和WFPUs乳胶膜力学性能测试结果 Tab. 5 Mechanical properties test results of WPU and WFPUs flims |
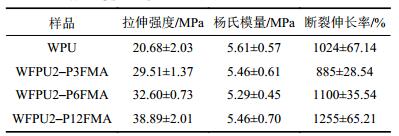 |
从表5可知,与WPU乳胶膜对比,WFPUs乳胶膜杨氏模量没有明显变化,表明引入含氟链段后,其抵抗形变的能力没有显著变化。随着含氟侧链长度增加,WFPUs乳胶膜断裂强度增加。这是因为随着含氟侧链长度增加,硬段的氢键作用增加,硬段的结晶度增加,从而使乳胶膜断裂强度增加。从该表还可知,除乳胶膜WFPU2–P3FMA,另外两种含氟乳胶膜的断裂伸长率均高于WPU,并且随着含氟侧链长度增加而提高。这是因为含氟链段引入后,促使形成更多氢键,对乳胶膜具有增强作用,在较低拉伸应力的作用下,增强的WFPUs乳胶膜的分子链段倾向于向应力方向排列并且软段的弹性形变没有受到阻碍,所以其断裂伸长率随着含氟侧链的长度的增加而增加。然而,在氟含量相同的条件下,由于WFPU2–P3FMA乳胶膜中的含氟侧链最多,大量的含氟侧链阻碍了软段的弹性形变,所以其断裂伸长率低于WPU乳胶膜。
3 结 论采用P3FMA、P6FMA和P12FMA改性WPUs,得到了3种侧链型WFPUs,分别为WFPUs–P3FMA、WFPUs–P6FMA和WFPUs–P12FMA。3种WFPUs乳胶膜的最低表面自由能分别是为34.78、32.41和15.94 mN/m,对应所需的最低氟含量分别为2%、1%、0.5%。XPS分析结果表明乳胶膜WFPUs–P12FMA的氟表面富集性能最好,所以引入少量含氟侧链长度最长的P12FMA即可显著降低表面自由,提高乳胶膜的疏水性能。由于硬段有序氢键化C=O含量随含氟侧链长度增加而增加,从而使硬段的结晶度增加,乳胶膜的断裂强度也随之提高,并且高于WPU乳胶膜。因此,侧链型WFPUs–P12FMA乳胶膜具有最好的疏水性能和力学性能。
| [1] |
Tonelli C,Ajroldi G. New fluoro-modified thermoplastic polyurethanes[J]. Journal of Applied Polymer Science, 2010, 87(14): 2279-2294. |
| [2] |
Turri S,Levi M,Trombetta T. Process design of fluorinated polyurethane-urea anionomer aqueous dispersions[J]. Macromolecular Symposia, 2004, 218(1): 29-38. |
| [3] |
Turri S,Levi M,Trombetta T. Waterborne anionomeric polyurethane-ureas from functionalized fluoropolyethers[J]. Journal of Applied Polymer Science, 2010, 93(1): 136-144. |
| [4] |
Lim H,Lee Y,Park I J,et al. Synthesis and surface property of aqueous fluorine-containing polyurethane[J]. Journal of Colloid Interface Science, 2001, 241(1): 269-274. DOI:10.1006/jcis.2001.7750 |
| [5] |
Zeng X,Ma Y,Wang Y. Enhancing the low surface energy properties of polymer films with a dangling shell of fluorinated block-copolymer[J]. Applied Surface Science, 2015, 338: 190-196. DOI:10.1016/j.apsusc.2015.02.134 |
| [6] |
Li J,Zhang X,Liu Z,et al. Studies on waterborne polyurethanes based on new medium length fluorinated diols[J]. Journal of Fluorine Chemistry, 2015, 175: 12-17. DOI:10.1016/j.jfluchem.2015.02.015 |
| [7] |
Wang S,Liu W,Tan J. Synthesis and properties of fluorine-containing polyurethane based on long chain fluorinated polyacrylate[J]. Journal of Macromolecular Science(Part A), 2016, 53(1): 41-48. DOI:10.1080/10601325.2016.1110456 |
| [8] |
Shin M,Lee Y,Rahman M,et al. Synthesis and properties of waterborne fluorinated polyurethane-acrylate using a solvent-/emulsifier-free method[J]. Polymer, 2013, 54(18): 4873-4882. DOI:10.1016/j.polymer.2013.07.005 |
| [9] |
Zhao M,Li H,Wen L,et al. Synthesis and characterization of fluorine-containing polyurethane-acrylate core-shell emulsion[J]. Journal of Applied Polymer Science, 2016, 133(17): 43357-43366. |
| [10] |
Owens D K,Wendt R. Estimation of the surface free energy of polymer[J]. Journal of Applied Polymer Science, 1969, 13(8): 1741-1747. DOI:10.1002/app.1969.070130815 |
| [11] |
Coleman M M,Skrovanek D J,Hu J B,et al. Hydrogen-bonding in polymer blends.1. FTIR studies of urethane ether blends[J]. Macromolecules, 1988, 21(1): 59-65. DOI:10.1021/ma00179a014 |
| [12] |
Luo N,Wang D N,Ying S K. Hydrogen-bonding properties of segmented polyether poly(urethane urea) copolymer[J]. Macromolecules, 1997, 30(15): 4405-4409. DOI:10.1021/ma951386e |
| [13] |
Ren Z Y,Wu H P,Ma J M,et al. FTIR studies on the model polyurethane hard segments based on a new waterborne chain extender dimethylol butanoic acid (DMBA)[J]. Chinese Journal of Polymer Science, 2004, 22(3): 225-230. |
| [14] |
Zhang S,Ren Z,He S,et al. FTIR spectroscopic characterization of polyurethane-urea model hard segments (PUUMHS) based on three diamine chain extenders[J]. Spectrochimica Acta Part a-Molecular and Biomolecular Spectroscopy, 2007, 66(1): 188-193. DOI:10.1016/j.saa.2006.02.041 |
| [15] |
Zharkov V V,Strikovsky A G,Verteletskaya T E. Amide-iabsorption-band-description of the urethane group association schemein polyether urethane elastomers[J]. Polymer, 1993, 34(5): 938-941. DOI:10.1016/0032-3861(93)90211-R |
| [16] |
Yoon S C,Ratner B D. Surface-structure of segmented poly(ether urethanes) and poly(ether urethane ureas) with various perfluoro chain extenders-an X-ray photoelectron spectroscopic investigation[J]. Macromolecules, 1986, 19(4): 1068-1079. DOI:10.1021/ma00158a023 |
| [17] |
Yoon S C,Ratner B D. Surface and bulk structure of segmented poly(ether urethanes) with perfluoro chain extenders. 2. FTIR,DSC,and X-ray photoelectron spectroscopic studies[J]. Macromolecules, 1988, 21(8): 2392-2400. DOI:10.1021/ma00186a016 |
| [18] |
Kolbeck C,Killian M,Maier F,et al. Surface characterization of functionalized imidazolium-based ionic liquids[J]. Langmuir, 2008, 24(17): 9500-9507. DOI:10.1021/la801261h |
| [19] |
Tan H,Xie X,Li J,et al. Synthesis and surface mobility of segmented polyurethanes with fluorinated side chains attached to hard blocks[J]. Polymer, 2004, 45(5): 1495-1502. DOI:10.1016/j.polymer.2003.12.068 |
| [20] |
Esteves A,Lyakhova K,Ven L,et al. Surface segregation of low surface energy polymeric dangling chains in a cross-linked polymer network investigated by a combined experimental-simulation approach[J]. Macromolecules, 2013, 46(5): 1993-2002. DOI:10.1021/ma302236w |
| [21] |
Park J H,Bae S Y,Kim B K. Hyperbranched waterborne polyurethanes[J]. Polymer Bulletin, 2013, 70(3): 859-869. DOI:10.1007/s00289-012-0891-y |
 2019, Vol. 51
2019, Vol. 51


