含酚废水常见于医药、石油化工、染料或者造纸行业,由于其兼具高毒性及生物难降解性,已成为废水净化研究的典型[1]。目前其降解技术研究中,以H2O2为氧化剂发展起来的湿式催化氧化技术(catalytic wet peroxide oxidation, CWPO)是热门,可以在温和条件下(如T<373 K,P=101.325 kPa)实现有机污染物向无毒产物CO2和H2O的转化,受到众多研究人员的关注[2]。
CWPO技术采用的催化剂可分为均相与非均相两类,以过渡金属离子为催化剂的均相湿式催化氧化技术应用广泛,但存在一定问题:对反应溶液pH的限制(如Fenton试剂需在pH<4使用)及催化剂易流失造成二次污染;同时额外的分离/回收工艺也增加了设备成本[3],而非均相催化剂在一定程度可以克服上述缺点。传统非均相催化剂以Cu系和Fe系催化剂的研究最为广泛[4],采用浸渍、水热合成及化学气相沉积等方法可以实现金属活性组分与固相载体的结合,获得低成本且催化性能优异的催化剂,然而活性组分流失的问题仍不容忽视。近年来碳质材料作为非金属催化剂成为了热点,石墨烯(graphene, Gr)[5]、碳纳米管(carbon nanotubes, CNTs)[6]、石墨及化学修饰活性炭[7]等均被证明同样可以催化氧化剂产生强氧化活性物质。其中CNTs具有高比表面积和孔体积,兼具一定的机械强度[8],在降解含酚废水的研究中已取得显著进展;而氮掺杂碳纳米管(nitrogen doped carbon nanotubes, NCNTs)被证明可以高效催化H2O2产生强氧化性活性物质,具有极大的研究潜力[9]。
含酚废水降解的实验研究多在搅拌槽式反应器中进行,操作便捷,且研究系统深入[10-11]。但反应不完全会导致高毒性的中间产物(如苯醌)的停留时间过长,存在安全隐患[12];同时由于剪切力的作用,催化剂活性组分易流失。在连续流动的固定床反应器上相关研究较少,然而后者可以在一定程度上克服上述问题,对于实现工业化处理具有重要意义[13]。由于粉末及颗粒状催化剂在固定床反应器上的装填会造成床层压降过高,工业上催化剂常需要胶黏成型[14],这易造成催化剂堵孔及比表面积下降。近年来又兴起对整体式材料的研究,通过吸附/涂覆/包覆/原位生长等方式可以实现活性组分与整体式载体(泡沫SiC和多孔Al2O3等陶瓷材料[15-16],不锈钢纤维和铜网等金属纤维[17],以及高分子膜材料[18]等)的结合,整合传热传质强化同高选择性/催化活性,构成适用于连续流动体系的结构单元,在催化重整[19],催化脱氢[20],气体净化[21]等领域均有应用。本课题组通过湿法造纸和烧结工艺制备了一种整体式纸状烧结不锈钢微纤载体[22](paper-like sintered stainless steel fibers, PSSF),具有高空隙率(>98%),耐腐蚀性及可任意裁剪的特性,同样可与固定床反应器很好地结合。
因此,作者通过化学气相沉积法(chemical vapor deposition, CVD),以低成本的三聚氰胺为单一的固体氮源和碳源在PSSF表面生长氮掺杂碳纳米管(NCNTs)以合成NCNTs/PSSF微纤复合材料,旨在将NCNTs优异的催化特性同PSSF的高空隙率、耐腐蚀性能相结合,以探究非金属负载型催化剂在含酚废水降解中的应用。
1 实验材料与方法 1.1 实验药品与试剂过氧化氢(30%),上海强顺化学试剂厂;苯酚(分析纯),广州化学试剂厂;甲醇(色谱纯),国药集团化学试剂有限公司;硫代硫酸钠(分析纯),天津博迪化工股份有限公司;盐酸(36%~38%),广州化学试剂厂;碘化钾(分析纯),天津博迪化工股份有限公司;三聚氰胺(分析纯),天津市科密欧化学试剂有限公司;不锈钢纤维(L=3 mm, D=6.5 μm),湖南惠同新材料有限公司。
1.2 实验仪器与装置固定床反应器(直径2 cm,长度10 cm),实验室自制;3–550马弗炉,美国VULCAN公司;Agilent1100高效液相色谱仪,美国安捷伦公司;S–3700N扫描电子显微镜,日本日立公司;JEM–2100F透射电子显微镜,日本电子株式会社;OTF–1200X管式炉,合肥科晶材料技术有限公司;Liqui TOC总有机碳分析仪,德国Elementar公司;AAS原子吸收光谱仪,美国Varian公司;STA449C热重分析仪,德国耐驰公司。
1.3 NCNTs/PSSF复合催化剂的制备PSSF纸状烧结不锈钢微纤材料的制备:1)采用湿法造纸工艺,以纤维素和不锈钢纤维(质量比1∶7)为原材料通过疏解、磨浆、抄纸等步骤制成纸状前体;2)采用煅烧工艺,程序升温在1 050 ℃下煅烧除去纸前体中的纤维素,后在马弗炉空气氛围中(550 ℃)二次煅烧,获得具有3维网状结构的PSSF微纤材料[23]。
NCNTs/PSSF复合催化剂的制备:以三聚氰胺为单一的碳源和氮源,采用化学气相沉积法进行NCNTs/PSSF的合成,制备工艺流程图如图1所示。将盛有PSSF的瓷舟置于管式炉加热段中部,盛有三聚氰胺的瓷舟置于加热区外,以恒温加热圈为辅助热源;之后在300 sccm氮气氛围中加热PSSF载体,达到指定温度后预热10 min;后开启辅助热源,使三聚氰胺在300 ℃下升华扩散,并在PSSF表面进行NCNTs的生长,反应时间为50 min。本研究将考察不同合成温度(800、900和1 000 ℃),不同氮气载气流量(50、100和300 sccm)及不同三聚氰胺用量(1、3和5 g)对NCNTs/PSSF复合催化剂合成工艺的影响。
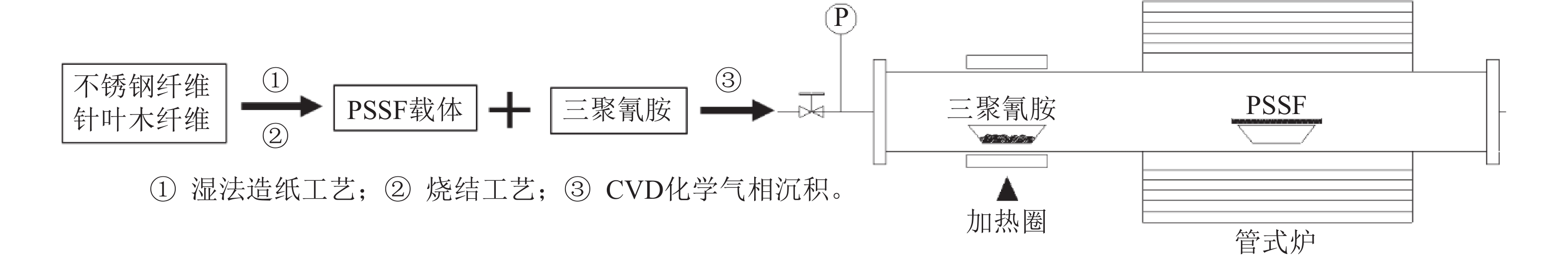 |
| 图1 制备工艺流程图 Fig. 1 Synthesis flow chart of catalyst |
1.4 催化性能评价 1.4.1 活性评价实验
NCNTs/PSSF复合催化剂对苯酚的湿式催化氧化过程在固定床反应器中进行。装置如图2所示,将裁剪成型的复合催化剂填充在反应器中段,两端装填相同床层高度的玻璃珠以固定催化剂。反应液配置为1 g/L苯酚同5.1 g/L H2O2的混合液(根据式(1)化学计量比计算总酚氧化所需H2O2),反应过程中控制反应温度为80 ℃,每隔1 h取出5 mL反应液用于进一步测定:
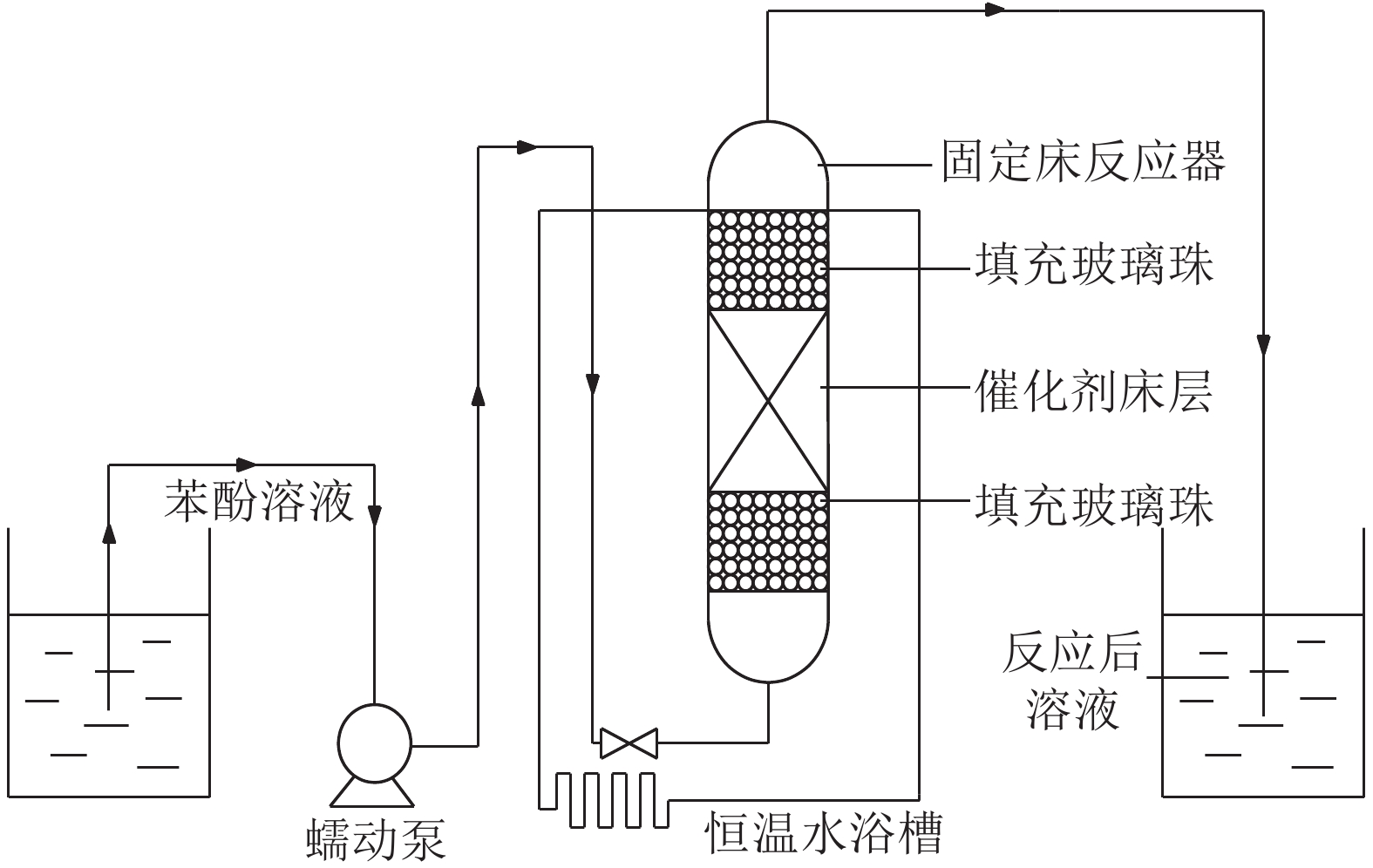 |
| 图2 装置流程图 Fig. 2 Flow chart of set-up |
| $ \rm {C_6}{H_5}OH + 14{H_2}{O_2} \xrightarrow{\;\;\;\;\;\;\;\;\;\;\;\;\;} 17{H_2}{\rm{O}} + 6C{O_2} $ | (1) |
取出的反应液在测定前首先稀释10倍,后进行相关催化性能指标的测定与计算:H2O2转化率计算通过间接碘量法实现;苯酚浓度采用高效液相色谱法(high performance liquid chromatography, HPLC)测定;TOC含量通过Liqui总有机碳分析仪测定;反应液中Fe3+的浓度由AAS原子吸收光谱仪进行测定[22]。
2 实验结果与讨论 2.1 NCNTs/PSSF复合催化剂的制备工艺 2.1.1 不同合成温度的影响在N2载气流量300 sccm,三聚氰胺用量3 g的条件下考察不同合成温度对NCNTs/PSSF复合催化剂表面形貌的影响。研究已证明PSSF载体具有发达三维网状结构,且不锈钢纤维间很好地烧结在一起[23],图3表明生长NCNTs后,纤维间仍保持着交联状态,同时纤维表面已环绕包裹着一层碳纳米管。随合成温度的上升(图3(b)、(c)、(d)),纤维表面的碳纳米管逐渐变长,一方面高温下三聚氰胺分解产生更多碳物种CNx(如NH3、HCN和CH4)[24],另一方面碳物种的扩散速率也在增加,促进了NCNTs的生长。而当温度上升至1 000 ℃时(图3(d)),纤维表面的管状物曲率变小,出现明显的团聚物,这是由于高温下碳物种在催化剂表面的沉积和扩散机理发生变化,使得碳纳米管向着石墨片层结构转化[25-26]。
 |
| 图3 不同合成条件对复合催化剂微观形貌的影响 Fig. 3 SEM images of NCNTs/PSSF composite catalyst synthesized under different conditions |
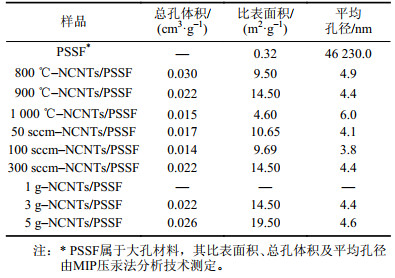
TG热重分析(图4(a))表明随着合成温度的上升,催化剂的失重率上升同时失重温度向高温区移动,说明纤维表面碳物质稳定性在提高;当失重率到达最高值后,各个条件下催化剂均出现增重的趋势,这是由于催化剂表面Fe物种发生进一步氧化所致。高空隙率的PSSF材料属于大孔结构,其比表面积由MIP(mercury intrusion porosimetry)压汞法分析测试仅为0.32 m2/g,由表1复合催化剂比表面积及孔结构分析可知,生长NCNTs后催化剂的比表面积显著提高,其中900 ℃下催化剂的比表面积最大,相比PSSF增加了近45倍。然而结合图4(a)同时可以观察到,比表面积随温度的变化趋势并不与TG热重分析一致,1 000 ℃条件下催化剂的失重率最高(23%)而比表面积反而最低(4.60 m2/g),这可能是由于高温下碳前驱物更多地形成了孔隙不发达的石墨片层结构所致[27]。
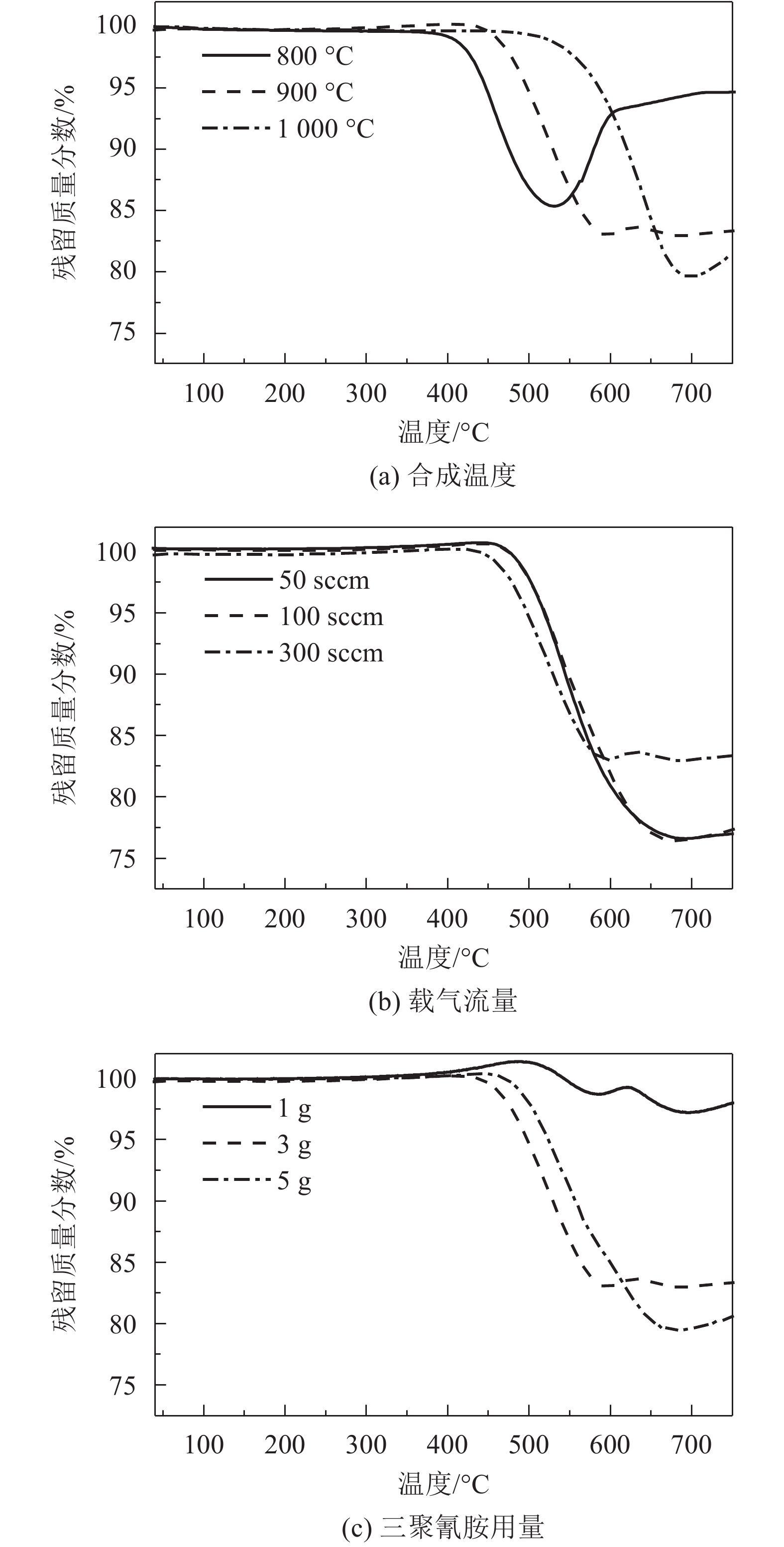 |
| 图4 不同合成条件下复合催化剂TG热重分析图 Fig. 4 TG analysis of NCNTs/PSSF composite catalyst synthesized under different conditions |
| 表1 样品的比表面积及孔结构分析 Tab. 1 Textural characteristics of the samples |
 |
进一步的Raman分析如图5(a)所示,所有样品均在拉曼位移约1 560 cm–1(G峰),1 350 cm–1(D峰)和2 700 cm–1(2D峰)处出现典型的碳纳米管峰型。可以明显观察到当合成温度较低时(800 ℃),D峰和G峰的分离度小,同时在1 180 cm–1处有明显的肩峰使D峰更宽,这是由于氮掺杂所致[28]。碳材料的缺陷程度可以由G峰和D峰强度比值(IG/ID)定性分析[29],而氮掺杂会导致石墨烯片层结构出现晶格缺陷[28],使该比值下降。随合成温度的上升,IG/ID由0.96上升至1.44,D峰与G峰分离度变大,说明碳纳米管的缺陷程度在下降;同时2D峰也在逐渐升高,说明碳纳米管的石墨化程度和有序度在上升。由以上表征结果可知,900 ℃是本研究合成NCNTs/PSSF复合催化剂的合适温度。
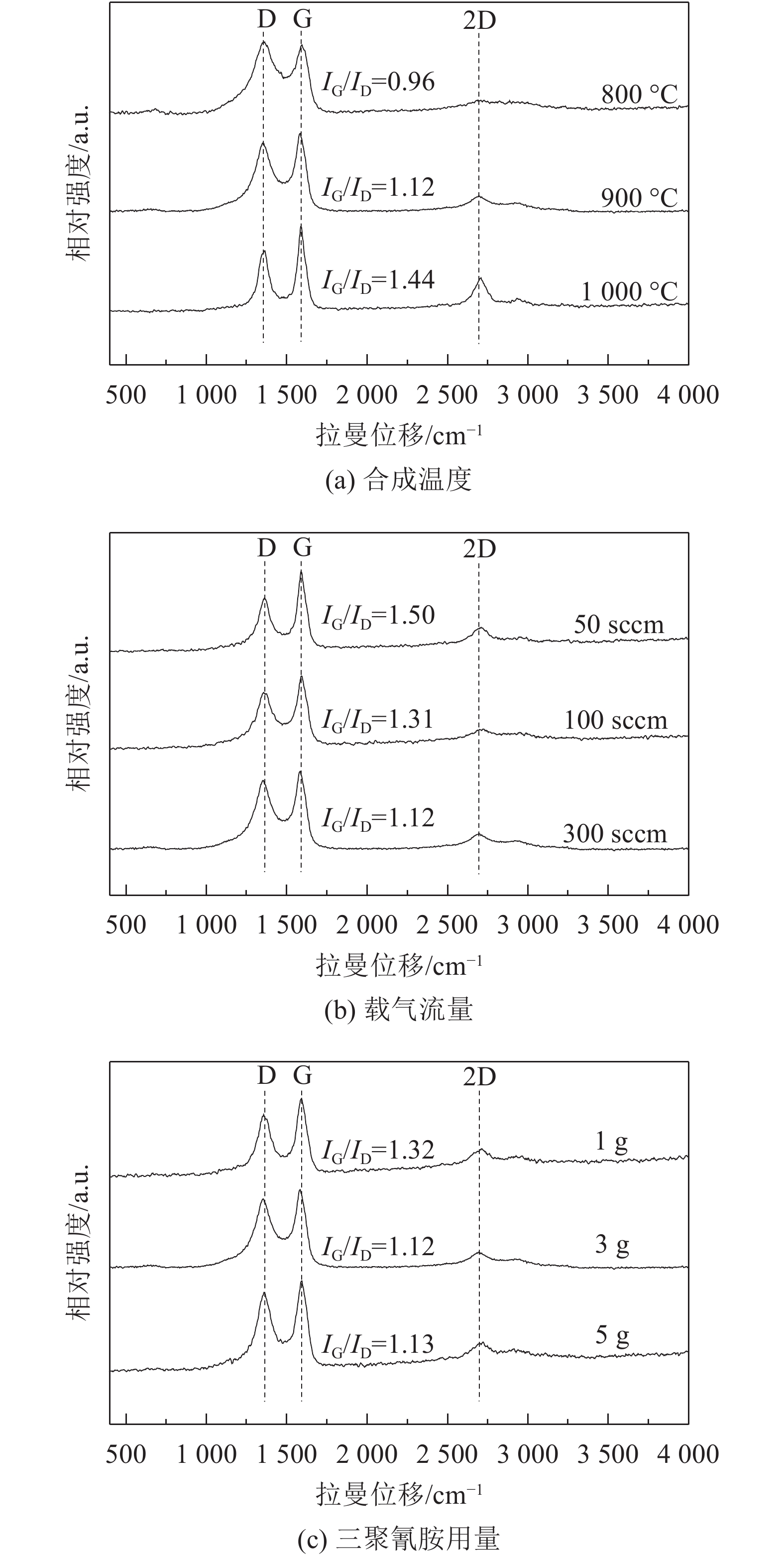 |
| 图5 不同合成条件下复合催化剂Raman谱图 Fig. 5 Raman spectra of NCNTs/PSSF composite catalyst synthesized under different conditions |
2.1.2 不同载气流量的影响
在合成温度900 ℃,三聚氰胺用量3 g的条件下考察不同N2载气流量对NCNTs/PSSF复合催化剂表面形貌的影响。由图3(b)可以观察到载气流量较低时(50 sccm)纤维表面的碳纳米管生长紧密且较短;当流量逐渐上升时(100 sccm),碳纳米管的长度有所增加,生长密度仍较高;而当流量继续上升时(300 sccm),虽然碳纳米管的长度增长明显,但生长密度明显下降。这可能是由于在低流量条件下,三聚氰胺分解产生的碳物种与纤维表面充分接触并占据绝大多数催化活性位点,使碳纳米管的生长密度较大,然而由于分解产生的碳物种分压过高,催化剂表面瞬间沉积过多的碳层,阻碍了碳析出生长为碳纳米管;而随着流量的提高,含碳物种的分压下降,催化剂表面的碳沉积和扩散速率相对平衡,碳纳米管生长稳定。但这也降低了碳前驱物与纤维表面的接触时间,使得碳纳米管的生长密度下降[30-31]。
TG热重分析(图4(b))表明,载气流量的变化对催化剂的热稳定性影响不明显,但影响碳纳米管的产量,低流量条件下气态的碳前驱物可以充分和纤维表面接触,进而生成更多的碳纳米管。结合表1可知,虽然300 sccm载气流量条件下催化剂表面碳纳米管生长密度较低,但仍获得最高的比表面积(14.50 m2/g)。
进一步的Raman分析如图5(b)所示,样品均出现典型的碳纳米管峰型。随着载气流量的上升,IG/ID值由1.50下降至1.12,说明缺陷程度在上升。正如之前提及,在较高载气流量(较低碳物种分压)条件下,碳纳米管的生长更为稳定,促进了C—N键在石墨层结构中的形成[31],带来更多的缺陷。结合以上表征结果可知,300 sccm N2流量是本研究合成NCNTs/PSSF复合催化剂的合适载气流量条件。
2.1.3 三聚氰胺用量的影响在合成温度900 ℃,N2载气流量300 sccm的条件下考察不同三聚氰胺用量对NCNTs/PSSF复合催化剂表面形貌的影响。由图3(c)可以观察到随三聚氰胺用量的上升,纤维表面碳纳米管的生长密度在提高,而长度没有明显的变化。三聚氰胺用量的提高产生了更多的碳物种,对纤维表面催化活性位点的利用率在提高。
TG热重分析(图4(c))表明,纤维表面碳纳米管的产量受碳源用量影响明显,随着三聚氰胺用量的提高,失重率上升明显(5%上升至20%)。由表1可知,比表面积与三聚氰胺的用量呈正相关。当用量仅为1 g时,复合催化剂比表面积值过低无法测出,结合热重分析,推测这可能是由于PSSF表面碳纳米管产量较低(失重率仅为5%),引起比表面积的增量值低于仪器的灵敏度所致。当三聚氰胺用量分别为3和5 g时,复合催化剂的比表面积相比PSSF载体分别提高了45倍和60倍,达到14.50和19.50 m2/g。
Raman分析(图5(c))表明,提高三聚氰胺的用量对合成的碳纳米管的缺陷情况影响并不大。考虑成本因素结合以上表征可知,用量3 g是本研究合成NCNTs/PSSF复合催剂的适宜碳源用量。
2.2 NCNTs/PSSF复合催化剂的TEM分析根据复合催化剂初步制备工艺的结果,本研究对在合成温度900 ℃,N2载气流量300 sccm及三聚氰胺用量3 g条件下合成的催化剂的微观形貌进行进一步分析。
由图6(a)高分辨率TEM图可知,PSSF载体表面生长的碳纳米管为多壁结构,呈现出明显的不规则和和相互嵌套的褶皱状形貌[28],这是由于氮原子进入碳纳米管原本有序的晶格结构而引起缺陷所致,说明已成功地在PSSF载体表面合成了氮掺杂碳纳米管,其中氮掺杂碳纳米管的管径在50~100 nm间,壁厚约为10 nm。由表2元素分析(即图6(b)标示处)可知氮掺杂的原子百分比约为4%。
 |
| 图6 复合催化剂TEM微观形貌分析 Fig. 6 TEM images of NCNTs/PSSF composite catalyst |
| 表2 样品TEM–EDS元素分析 Tab. 2 TEM–EDS element analysis of the sample |
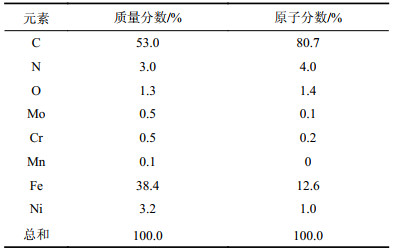 |
图6(b)对NCNTs的内部结构进行进一步分析,可以看到催化剂颗粒被包裹在管腔内,这些催化剂颗粒是高温条件下不锈钢纤维表面发生拉伸破碎而形成的,同时在NCNTs的生长过程中受到挤压从而进入了管腔中[32]。结合图6(b)和表2元素分析可知催化剂颗粒的主要金属成分是Fe,而不是Ni或者Cr,这与Pattinson等[33]的研究结果一致,说明Fe物种是催化NCNTs生长的关键。
2.3 NCNTs/PSSF复合催化剂催化性能评价将最优工艺下制备的NCNTs/PSSF复合催化剂用于固定床反应器上苯酚的湿式催化氧化降解过程,以空载体PSSF为对照组。其中催化剂床层高度为2 cm(约含有0.5 g的NCNTs),反应流量2 mL/min,反应温度为80 ℃,反应时间9 h。考察反应过程中H2O2、苯酚、TOC转化率及溶液pH随时间的变化关系,由于PSSF载体表面经过高温煅烧会形成了一层Fe2O3氧化膜,因此研究同时对反应过程中Fe3+的浸出浓度进行分析,结果如图7(a)~(e)所示。
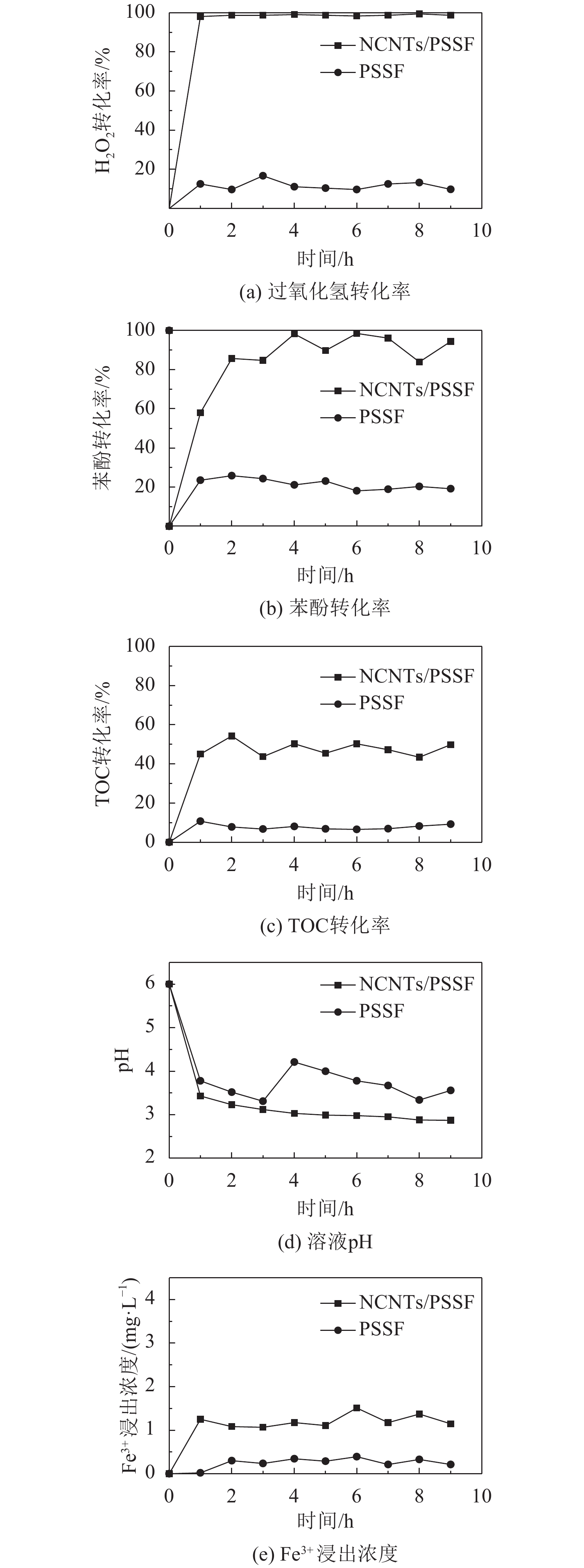 |
| 图7 H2O2转化率、苯酚转化率、TOC转化率及溶液pH、Fe3+的浸出浓度随时间变化曲线 Fig. 7 Profiles of hydrogen peroxide conversion,phenol conversion,TOC conversion,solution pH and Fe3+ leaching concentration with time |
观察图7(a),PSSF空载体可以达到约15%的H2O2转化率,可能是由于其表面存在的Fe2O3氧化膜对H2O2的分解有一定催化作用[34],并且H2O2本身也会部分分解生成O2。当在PSSF表面生长NCNTs后,NCNTs/PSSF复合催化剂可以高效催化H2O2,转化率达到99%并维持至反应结束。这是由于氮掺杂使NCNTs具有更多缺陷活性位点和给电子特性,可以高效吸附极性H2O2并促进其分解[9]。
观察图7(b),复合催化剂可以达到良好的苯酚降解效率(>80%),且随着时间推移转化率没有明显的下降,而空载体仅能达到20%的苯酚转化率。虽然载体本身降解效率不佳,但其3维网状结构和高空隙率,可以减少外扩散阻力,提高传质效率;而当NCNTs作为2维材料均匀分散在纤维表面时,在连续流动的系统中极大地提高了反应接触面积,增强了催化效果。
观察图7(c),生长NCNTs后复合催化剂对苯酚的矿化能力由10%提高到了45%。残留的TOC值通常是由于苯酚不完全降解形成中间产物所致。此外,由图7(d)可以明显观察到反应液的pH随时间变化逐渐下降,说明部分苯酚降解形成酸性副产物。
观察图7(e),反应中PSSF空载体的Fe3+浸出浓度约为0.5 mg/L,表现出其优良的耐腐蚀性能。而NCNTs/PSSF复合催化剂在反应过程中Fe3+浸出浓度仍保持极低的水平,约为1.5 mg/L,低于大多数Fe系催化剂的浸出结果[34-37]。低Fe3+浸出有两部分原因:1)虽然碳纳米管内包裹着催化剂颗粒,但内容物的溶出往往需要强酸以破坏碳纳米管的端口[38];2)三聚氰胺分解产物中存在—C≡N键,有助于稳定碳物种组装成稳定的SP2杂化结构,从而减少包裹有催化剂颗粒的无定型碳团簇的形成,进一步降低了酸性条件下Fe物种的浸出[31,39]。
采用HPLC高效液相色谱分析技术对NCNTs/PSSF复合催化剂催化氧化降解苯酚过程的中间产物进行分析,结果如图8所示。可以观察到在反应初期(0~3 h),随时间上升苯酚的特征峰强度下降,而中间产物峰有所增强,之后趋于稳定。这是因为在HO•的作用下,苯酚首先发生亲电加成并被降解为其他芳香族中间产物(如苯醌、对苯二酚、邻苯二酚和间苯二酚);之后HO•继续进攻苯环的共轭结构,使其断裂形成其他氧化副产物(主要是小分子羧酸)。图8中保留时间在2.6、3.7、4.6及5.6 min左右出现的峰分别属于深度氧化形成的小分子羧酸、苯醌、对苯二酚和邻苯二酚的色谱峰[40],这也与图7(d)描述一致。
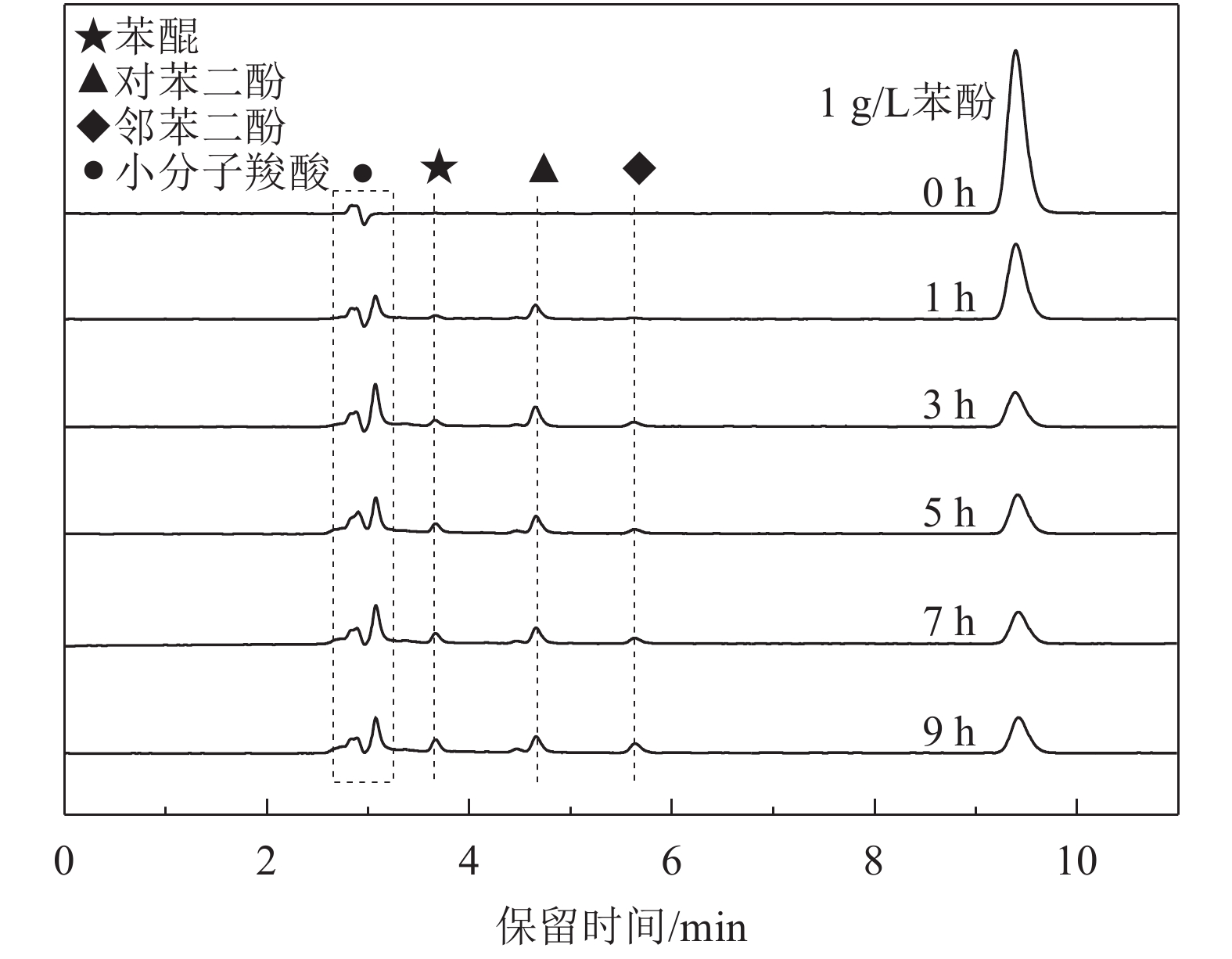 |
| 图8 不同时间条件下反应液的高效液相色谱分析 Fig. 8 HPLC analysis of the treated solution under different time |
虽然NCNTs/PSSF复合催化剂可以达到80%的苯酚转化率,但TOC转化率相对较低(45%),这可能是由于:1)苯酚在降解过程中形成的中间产物对HO•自由基有清除作用;2)中间产物与H2O2发生NCNTs表面活性位点的竞争吸附[41],阻碍H2O2高效转化为HO•;3)此外,降解产生的小分子羧酸由于经过高度氧化,进一步的降解也更困难[42]。
2.4 NCNTs/PSSF复合催化剂稳定性评价为了考察催化剂的稳定性,重新制备了NCNTs/PSSF复合催化剂并进行稳定性测试,反应条件为:催化剂床层高度2 cm(约0.5 g NCNTs),反应温度80 ℃,反应流量2 mL/min,反应时间100 h。考察H2O2、苯酚转化率及Fe3+浸出浓度随时间的变化关系,见图9。
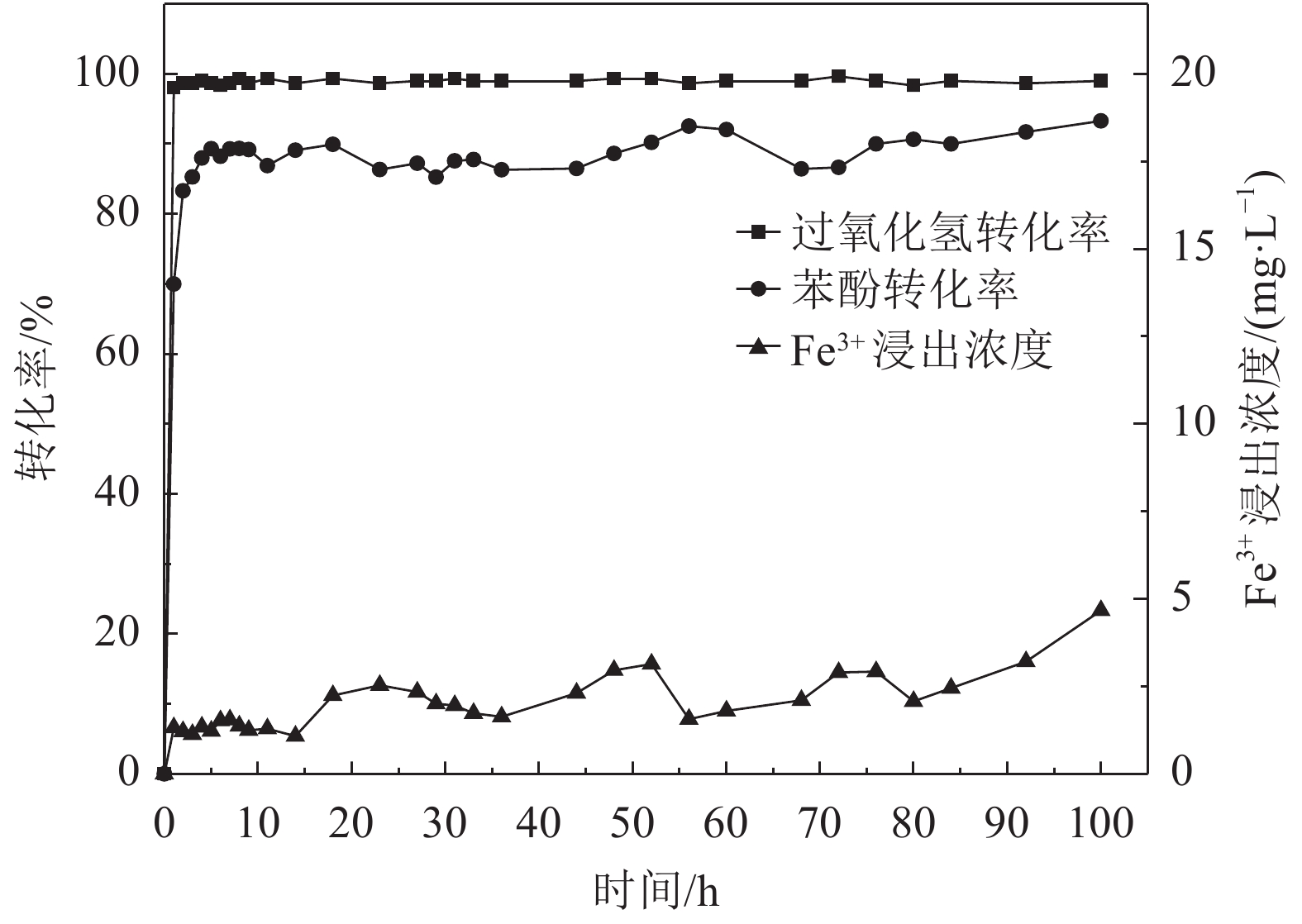 |
| 图9 NCNTs/PSSF复合催化剂长期稳定性测试 Fig. 9 Long term catalytic performance of NCNTs/PSSF composite catalyst |
由图9可知,在100 h反应过程中H2O2转化率保持在99%以上,苯酚转化率保持在80%以上,Fe3+浸出浓度有所上升,但仍保持较低水平(小于5 mg/L),说明NCNTs/PSSF复合催化剂具有优良的催化稳定性。
Ribeiro等[43]的研究曾指出在基于搅拌槽反应器的湿式催化氧化体系中,粉末NCNTs(氮掺杂含量约为5%)催化降解污染物效果并不理想,研究表明NCNTs的缺陷位点有助于催化H2O2分解产生强氧化性的HO•,但其强亲水性会导致优先吸附H2O2,阻断了污染物与HO•的结合,最终使H2O2与HO•重新结合形成H2O和O2。相较粉末NCNTs,NCNTs/PSSF复合催化剂具有3维网状结构,空隙率达80%以上,有效减少外扩散阻力,提高传质效率;而NCNTs作为2维材料均匀分散在纤维表面,在连续流动的系统中极大地提高了反应接触面积,相较粉末状NCNTs降低了内扩散的影响,从而增强了催化剂与反应液的接触效率,进而改善对苯酚的降解效果。
3 结 论以价格低廉的三聚氰胺为单一碳源和氮源,采用CVD化学气相沉积法成功地在PSSF不锈钢微纤载体表面生长NCNTs制备了NCNTs/PSSF复合催化剂,并探究了不同合成条件对复合催化剂的影响:
1)合成温度的上升可以提高纤维表面NCNTs的生长密度及长度,但过高的温度会促进碳管的石墨化程度,使其向石墨片层结构转变。
2)载气流量的上升会使纤维表面NCNTs的生长密度有所降低,而长度有所提高。这是因为载气流量的上升减少了三聚氰胺分解产生的碳物种与纤维活性表面的接触,但同时也提高了碳纳米管生长时碳物种的扩散速率。
3)三聚氰胺用量的上升可以提高纤维表面NCNTs的生长密度,但对其长度及缺陷程度没有明显影响。
在本研究最佳合成条件下(反应温度900 ℃,N2载气流量300 sccm,三聚氰胺用量3 g),NCNTs/PSSF复合催化剂的氮原子掺杂量可达到4%。固定床反应器上湿式催化氧化降解苯酚的结果表明,在NCNTs含量仅为0.5 g条件下,非金属负载型NCNTs/PSSF复合催化剂具有良好的催化活性及稳定性,反应100 h仍可保持80%以上的苯酚转化率;同时Fe3+浸出浓度较低(低于5 mg/L)。本研究认为NCNTs/PSSF复合催化剂的高空隙率和3维网状结构提高了其与反应液的接触效率,从而更好地发挥了NCNTs的催化特性。
| [1] |
Busca G,Berardinelli S,Resini C,et al. Technologies for the removal of phenol from fluid streams:A short review of recent developments[J]. Journal of Hazardous Materials, 2008, 160(2/3): 265-288. DOI:10.1016/j.jhazmat.2008.03.045 |
| [2] |
Rey A,Hungria A B,Duran-Valle C J,et al. On the optimization of activated carbon-supported iron catalysts in catalytic wet peroxide oxidation process[J]. Applied Catalysis (B):Environmental, 2016, 181: 249-259. DOI:10.1016/j.apcatb.2015.07.051 |
| [3] |
Cherkezova-Zheleva Z,Paneva D,Tsvetkov M,et al. Preparation of improved catalytic materials for water purification[J]. Hyperfine Interactions, 2014, 226(1/2/3): 517-527. DOI:10.1007/s10751-013-0976-5 |
| [4] |
Taran O P,Yashnik S A,Ayusheev A B,et al. Cu-containing MFI zeolites as catalysts for wet peroxide oxidation of formic acid as model organic contaminant[J]. Applied Catalysis B:Environmental, 2013, 140/141: 506-515. DOI:10.1016/j.apcatb.2013.04.050 |
| [5] |
Yoo J M,Park B,Kim S J,et al. Catalytic degradation of phenols by recyclable CVD graphene films[J]. Nanoscale, 2018, 10: 5840-5844. DOI:10.1039/C8NR00045J |
| [6] |
Pinho M T,Gomes H T,Ribeiro R S,et al. Carbon nanotubes as catalysts for catalytic wet peroxide oxidation of highly concentrated phenol solutions:towards process intensification[J]. Applied Catalysis (B):Environmental, 2015, 165: 706-714. DOI:10.1016/j.apcatb.2014.10.057 |
| [7] |
Domínguez C M,Ocón P,Quintanilla A,et al. Graphite and carbon black materials as catalysts for wet peroxide oxidation[J]. Applied Catalysis (B):Environmental, 2014, 144: 599-606. DOI:10.1016/j.apcatb.2013.07.069 |
| [8] |
Ribeiro R S,Silva A M T,Figueiredo J L,et al. Removal of 2–nitrophenol by catalytic wet peroxide oxidation using carbon materials with different morphological and chemical properties[J]. Applied Catalysis B:Environmental, 2013, 140/141: 356-362. DOI:10.1016/j.apcatb.2013.04.031 |
| [9] |
Voitko K V,Whitby R L D,Gun’ko V M,et al. Morphological and chemical features of nano and macroscale carbons affecting hydrogen peroxide decomposition in aqueous media[J]. Journal of Colloid and Interface Science, 2011, 361(1): 129-136. DOI:10.1016/j.jcis.2011.05.048 |
| [10] |
Ramírez J H,Galeano L A,Pinchao G,et al. Optimized CWPO phenol oxidation in CSTR reactor catalyzed by Al/Fe–PILC from concentrated precursors at circumneutral pH[J]. Journal of Environmental Chemical Engineering, 2018, 6(2): 2429-2441. DOI:10.1016/j.jece.2018.02.024 |
| [11] |
Sashkina K A,Parkhomchuk E V,Rudina N A,et al. The role of zeolite Fe–ZSM–5 porous structure for heterogeneous Fenton catalyst activity and stability[J]. Microporous and Mesoporous Materials, 2014, 189: 181-188. DOI:10.1016/j.micromeso.2013.11.033 |
| [12] |
Inchaurrondo N,Cechini J,Font J,et al. Strategies for enhanced CWPO of phenol solutions[J]. Applied Catalysis (B):Environmental, 2012, 111/112: 641-648. DOI:10.1016/j.apcatb.2011.11.019 |
| [13] |
Taran O P,Zagoruiko A N,Ayusheev A B,et al. Wet peroxide oxidation of phenol over Cu– ZSM– 5 catalyst in a flow reactor.Kinetics and diffusion study[J]. Chemical Engineering Journal, 2015, 282: 108-115. DOI:10.1016/j.cej.2015.02.064 |
| [14] |
Martínez F,Melero J A,Botas J,et al. Treatment of phenolic effluents by catalytic wet hydrogen peroxide oxidation over Fe2O3/SBA–15 extruded catalyst in a fixed-bed reactor
[J]. Industrial & Engineering Chemistry Research, 2007, 46(13): 4396-4405. DOI:10.1021/ie070165h |
| [15] |
Jiao Y,Ou X,Zhang J,et al. Structured ZSM–5 coated SiC foam catalysts for process intensification in catalytic cracking of n-hexane[J]. Reaction Chemistry & Engineering, 2019, 4: 427-435. DOI:10.1039/C8RE00215K |
| [16] |
Chen P,Zhao G,Liu Y,et al. Monolithic Ni5Ga3/SiO2/Al2O3/Al-fiber catalyst for CO2 hydrogenation to methanol at ambient pressure
[J]. Applied Catalysis (A):General, 2018, 562: 234-240. DOI:10.1016/j.apcata.2018.06.021 |
| [17] |
Wang H,Dong Z,Na C. Hierarchical carbon nanotube membrane-supported gold nanoparticles for rapid catalytic reduction of p-Nitrophenol[J]. ACS Sustainable Chemistry & Engineering, 2013, 1(7): 746-752. DOI:10.1021/sc400048m |
| [18] |
Macanás J,Ouyang L,Bruening M L,et al. Development of polymeric hollow fiber membranes containing catalytic metal nanoparticles[J]. Catalysis Today, 2010, 156(3/4): 181-186. DOI:10.1016/j.cattod.2010.02.036 |
| [19] |
Luneau M,Gianotti E,Guilhaume N,et al. Experiments and modeling of methane autothermal reforming over structured Ni–Rh–Based Si–SiC foam catalysts[J]. Industrial & Engineering Chemistry Research, 2017, 56(45): 13165-13174. DOI:10.1021/acs.iecr.7b01559 |
| [20] |
Feng L,Liu Y,Jiang Q,et al. Nanodiamonds @ N,P co-modified mesoporous carbon supported on macroscopic SiC foam for oxidative dehydrogenation of ethylbenzene[J]. Catalysis Today, 2019, 18(2): 46. DOI:10.1016/j.cattod.2019.02.046 |
| [21] |
Nacken M,Ma L,Heidenreich S,et al. Development of a catalytic ceramic foam for efficient tar reforming of a catalytic filter for hot gas cleaning of biomass-derived syngas[J]. Applied Catalysis (B):Environmental, 2012, 125: 111-119. DOI:10.1016/j.apcatb.2012.05.027 |
| [22] |
Yan Y,Jiang S,Zhang H,et al. Preparation of novel Fe–ZSM–5 zeolite membrane catalysts for catalytic wet peroxide oxidation of phenol in a membrane reactor[J]. Chemical Engineering Journal, 2015, 259: 243-251. DOI:10.1016/j.cej.2014.08.018 |
| [23] |
Chen H,Zhang H,Yan Y. Preparation and characterization of a novel gradient porous ZSM–5 zeolite membrane/PSSF composite and its application for toluene adsorption[J]. Chemical Engineering Journal, 2012, 209: 372-378. DOI:10.1016/j.cej.2012.08.020 |
| [24] |
Wu X,Tao Y,Lu Y,et al. High-pressure pyrolysis of melamine route to nitrogen-doped conical hollow and bamboo-like carbon nanotubes[J]. Diamond and Related Materials, 2006, 15(1): 164-170. DOI:10.1016/j.diamond.2005.09.018 |
| [25] |
Shinde S M,Kano E,Kalita G,et al. Grain structures of nitrogen-doped graphene synthesized by solid source-based chemical vapor deposition[J]. Carbon, 2016, 96: 448-453. DOI:10.1016/j.carbon.2015.09.086 |
| [26] |
Wang Z,Li P,Chen Y,et al. Synthesis of nitrogen-doped graphene by chemical vapour deposition using melamine as the sole solid source of carbon and nitrogen[J]. Journal of Materials Chemistry (C), 2014, 2(35): 7396-7401. DOI:10.1039/c4tc00924j |
| [27] |
Yan H,Chen Y,Xu S. Synthesis of graphitic carbon nitride by directly heating sulfuric acid treated melamine for enhanced photocatalytic H2 production from water under visible light
[J]. International Journal of Hydrogen Energy, 2012, 37(1): 125-133. DOI:10.1016/j.ijhydene.2011.09.072 |
| [28] |
Sharifi T,Nitze F,Barzegar H R,et al. Nitrogen doped multi walled carbon nanotubes produced by CVD-correlating XPS and Raman spectroscopy for the study of nitrogen inclusion[J]. Carbon, 2012, 50(10): 3535-3541. DOI:10.1016/j.carbon.2012.03.022 |
| [29] |
Chen L,Li Z,Chen Z,et al. Three-dimensional nitrogen-doped carbon nanotubes/carbon nanofragments complexes for efficient metal-free electrocatalyst towards oxygen reduction reaction[J]. International Journal of Hydrogen Energy, 2018, 43(12): 6158-6166. DOI:10.1016/j.ijhydene.2018.02.010 |
| [30] |
Pal S K,Talapatra S,Kar S,et al. Time and temperature dependence of multi-walled carbon nanotube growth on Inconel 600[J]. Nanotechnology, 2008, 19(4): 045610. DOI:10.1088/0957-4484/19/04/045610 |
| [31] |
Malek Abbaslou R M,Soltan J,Dalai A K. The effects of carbon concentration in the precursor gas on the quality and quantity of carbon nanotubes synthesized by CVD method[J]. Applied Catalysis (A):General, 2010, 372(2): 147-152. DOI:10.1016/j.apcata.2009.10.025 |
| [32] |
Camilli L,Scarselli M,Del Gobbo S,et al. The synthesis and characterization of carbon nanotubes grown by chemical vapor deposition using a stainless steel catalyst[J]. Carbon, 2011, 49(10): 3307-3315. DOI:10.1016/j.carbon.2011.04.014 |
| [33] |
Pattinson W S,Balakrishnan V N,Zakharov D,et al. Mechanism and enhanced yield of carbon nanotube growth on stainless steel by oxygen-induced surface reconstruction[J]. Chemistry of Materials, 2015, 27(3): 932-937. DOI:10.1021/cm504209u |
| [34] |
Liu P,He S,Wei H,et al. Characterization of α–Fe2O3/γ–Al2O3 catalysts for catalytic wet peroxide oxidation of m-cresol
[J]. Industrial & Engineering Chemistry Research, 2015, 54(1): 130-136. DOI:10.1021/ie5037897 |
| [35] |
Dhakshinamoorthy A,Navalon S,Alvaro M,et al. Metal nanoparticles as heterogeneous Fenton catalysts[J]. ChemSusChem, 2012, 5(1): 46-64. DOI:10.1002/cssc.201100517 |
| [36] |
Rey A,Faraldos M,Casas J A,et al. Catalytic wet peroxide oxidation of phenol over Fe/AC catalysts:Influence of iron precursor and activated carbon surface[J]. Applied Catalysis (B):Environmental, 2009, 86(1/2): 69-77. DOI:10.1016/j.apcatb.2008.07.023 |
| [37] |
Botas J A,Melero J A,Martínez F,et al. Assessment of Fe2O3/SiO2 catalysts for the continuous treatment of phenol aqueous solutions in a fixed bed reactor
[J]. Catalysis Today, 2010, 149(3/4): 334-340. DOI:10.1016/j.cattod.2009.06.014 |
| [38] |
Pan X,Bao X. Reactions over catalysts confined in carbon nanotubes[J]. Chemical Communications, 2008, 47: 6271. DOI:10.1039/B810994J |
| [39] |
Wang Z,Jia R,Zheng J,et al. Nitrogen-promoted self-assembly of N-doped carbon nanotubes and their intrinsic catalysis for oxygen reduction in fuel cells[J]. ACS Nano, 2011, 5(3): 1677-1684. DOI:10.1021/nn1030127 |
| [40] |
Huang Y,Tian X,Nie Y,et al. Enhanced peroxymonosulfate activation for phenol degradation over MnO2 at pH 3.5–9.0 via Cu(Ⅱ) substitution
[J]. Journal of Hazardous Materials, 2018, 360: 303-310. DOI:10.1016/j.jhazmat.2018.08.028 |
| [41] |
Domínguez C M,Ocón P,Quintanilla A,et al. Highly efficient application of activated carbon as catalyst for wet peroxide oxidation[J]. Applied Catalysis B:Environmental, 2013, 140/141: 663-670. DOI:10.1016/j.apcatb.2013.04.068 |
| [42] |
Zazo J A,Casas J A,Mohedano A F,et al. Catalytic wet peroxide oxidation of phenol with a Fe/active carbon catalyst[J]. Applied Catalysis B:Environmental, 2006, 65(3): 261-268. DOI:10.1016/j.apcatb.2006.02.008 |
| [43] |
Ribeiro R S,Silva A M T,Pastrana-Martínez L M,et al. Graphene-based materials for the catalytic wet peroxide oxidation of highly concentrated 4-nitrophenol solutions[J]. Catalysis Today, 2015, 249: 204-212. DOI:10.1016/j.cattod.2014.10.004 |
 2019, Vol. 51
2019, Vol. 51


