2. 华北电力大学 可再生能源学院 生物质发电成套设备国家工程实验室,北京 102206
2. National Eng. Lab. for Biomass Power Generation Equipment, School of Renewable Energy, North China Electric Power Univ., Beijing 102206, China
化学链燃烧(chemical looping combustion,CLC)是一种可实现低成本CO2捕集的新型燃烧技术[1]。利用不断循环于空气反应器(AR)和燃料反应器(FR)之间的载氧体,如图1所示,将空气中的氧以晶格氧的形式传递给燃料,避免了烟气被N2稀释,从而实现了烟气中CO2的内分离,极大减少碳分离成本。此外,CLC技术还具备低NOx生成和能量梯级高效利用等优点[2]。
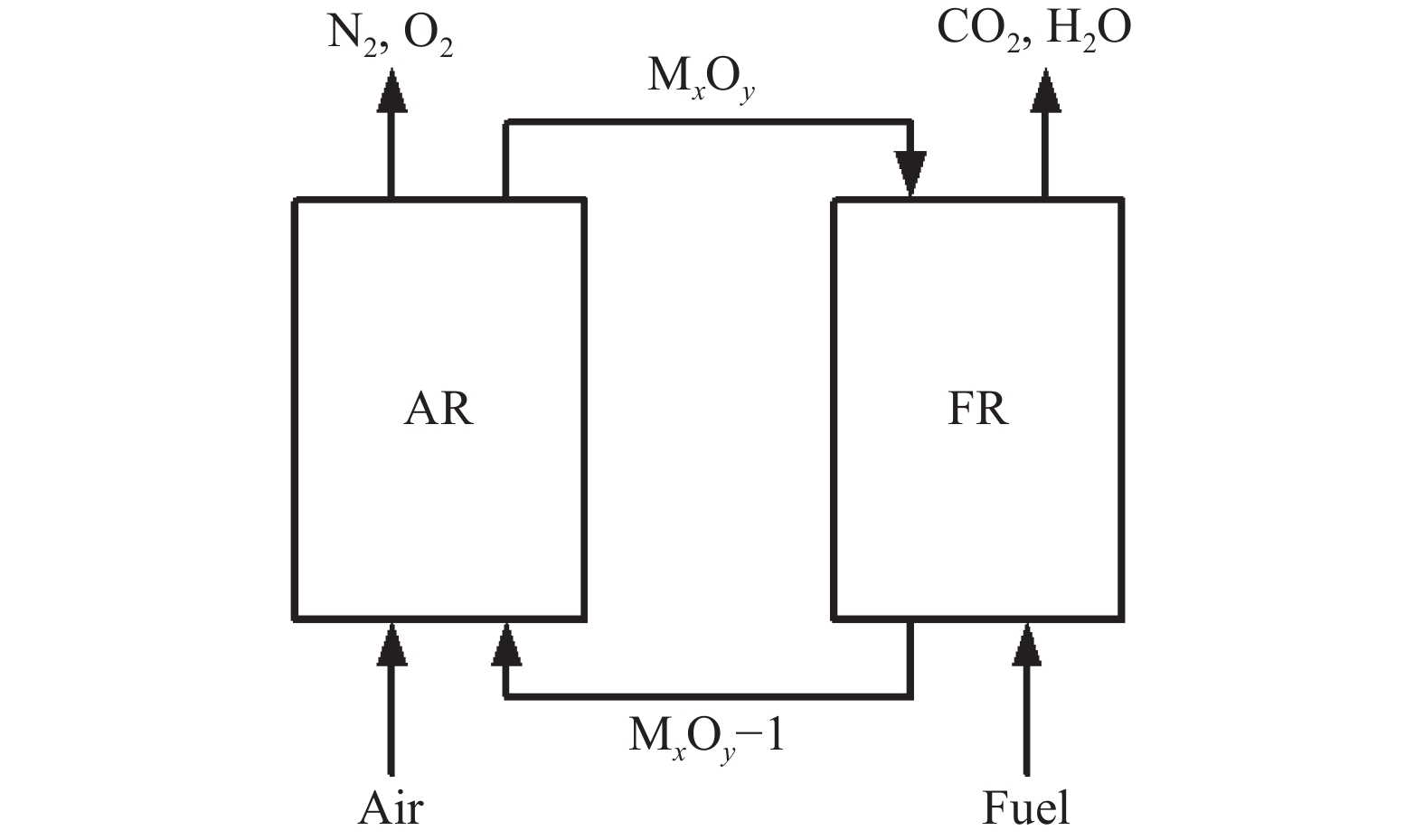 |
| 图1 化学链燃烧系统概念图 Fig. 1 Schematic of chemical looping combustion |
在CLC中,载氧体的性能是决定化学链燃烧系统性能的关键因素之一[3]。目前,研究较多的载氧体主要包括金属载氧体和非金属载氧体两大类。金属氧化物作为主流载氧体具有反应速度快、耐高温等优点,主要有Ni、Cu、Fe、Co、Mn等过渡金属的氧化物[4]。然而,单一金属氧化物载氧体各具优缺点,难以满足CLC技术的实际应用。例如,Ni基载氧体反应活性高、抗烧结能力强、载氧量大,但稳定性差、价格高、易析碳、对环境有害[5];Cu基载氧体反应活性较高、载氧能力强,但价格高、易烧结[6];Fe基载氧体价格低、来源广、环境友好、热稳定好,但反应活性和载氧能力较低[7-8]。因此,基于金属氧化物的优点以及相互间的协同作用,有学者提出了通过掺杂高活性成分提高铁基载氧体反应活性的方法,并取得了较高活性的铁基载氧体[9]。
掺杂改性载氧体在化学链燃烧中表现出了较高的物理和化学性质。Miller等[10]指出CH4与掺杂CeO2的Fe2O3反应时,首先与CeO2反应生成CO和H2,然后在与Fe2O4反应,大幅减少了积碳的生成。顾海明等[11]发现钾基修饰后的铁矿石与煤反应时间缩短,气体产物浓度上升且含碳气体体积比下降。张思文等[12]研究表明碱金属Na和过渡金属Ni可以提高铁矿石载氧体的反应活性,但多次反应后Na流失比较严重。Hossain等[13]表明掺杂Co后H2与Ni/Al2O3载氧体反应的活化能减小,反应速率加快。覃吴等[14-15]研究发现Co–Fe2O3载氧体在CO及褐煤的化学链燃烧过程中较未改性的铁基载氧体活性要高。以上研究表明,掺杂高性组分可以改善铁基载氧体反应活有帮助。然而掺杂的部分活性组分在一定程度上会降低载氧体的热稳定性[16]。
目前,掺杂改性铁基载氧体的研究主要通过实验方法制备和性能表征,不仅需要使用多种仪器设备,开展大量制备和表征等实验,而且难以从分子层面了解微观的掺杂和反应机理。因此,作者基于密度泛函理论(density functional theory,DFT)展开Co掺杂对Fe2O3结构及其在CO氧化反应过程中的改性机理。相比于实验研究,理论模拟能够完成很多受实验条件限制而无法进行的研究工作,并且具有低成本性、不可替代性和较好的可控性等特点[17]。因此本研究旨在快速准确的从原子和分子层面研究Co对Fe2O3的改性机制,为载氧体反应性能的优化提供理论参考,减少实验过程中资源消耗和时间成本。
1 模型与计算方法 1.1 Co–Fe2O3(104)模型的建立α–Fe2O3的晶胞参数为:a=b=0.503 5 nm,c=1.374 7 nm;α=β=90°,γ=120°,如图2所示。Sandratskii等[18]在研究Fe2O3的电磁性能过程中对比多种自旋方式,发现以(+,-,-,+)自旋态设定得到Fe2O3斜方六面体晶胞结构,能量最低,结构最稳定。因此,在Fe2O3斜方六面体晶胞结构中,Fe原子在z轴方向的自旋态设定为(+,-,-,+),其中+和-分别对应自旋向上和自旋向下。沿着(104)方向切割Fe2O3的晶胞,得到具有周期性结构Fe2O3(104)的表面模型。为了消除表面中层与层之间的相互作用,真空层取1.2 nm。几何优化后得到Fe2O3(104)稳定模型,再以Co原子替换表面的Fe原子,经几何优化得到Co掺杂的Fe2O3(104)模型。
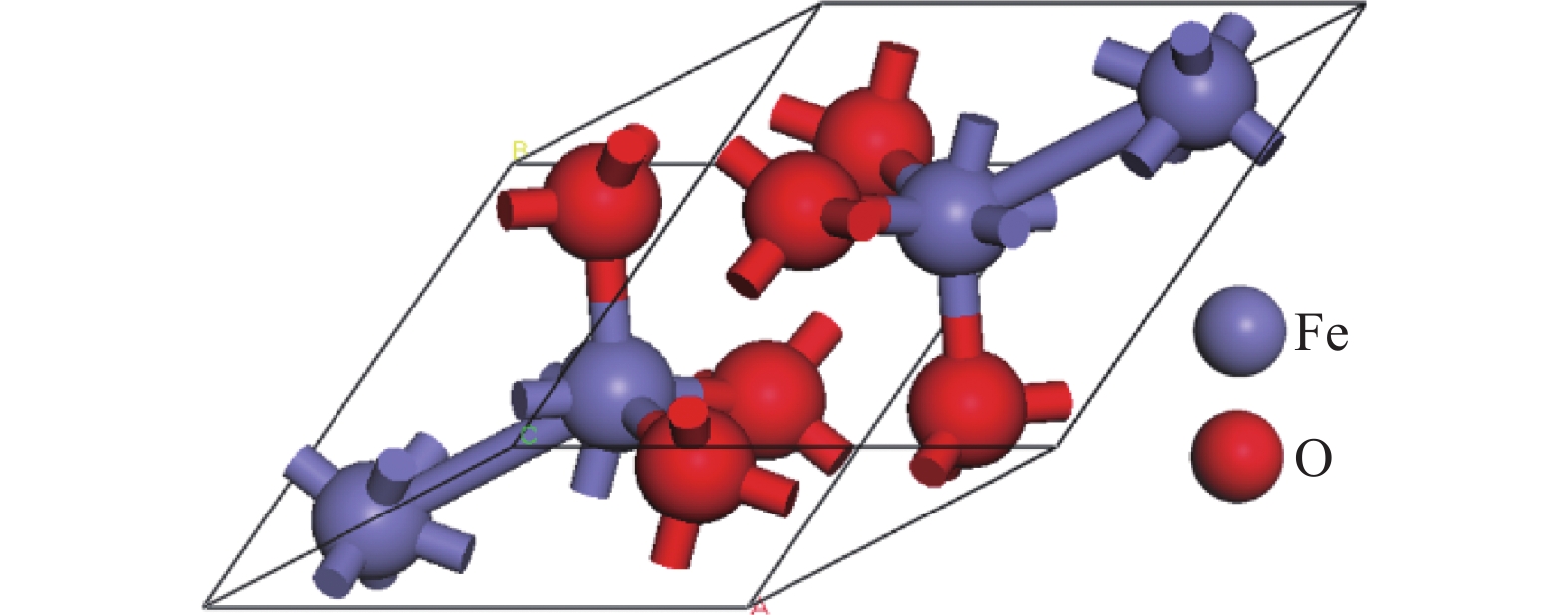 |
| 图2 α–Fe2O3的晶胞结构 Fig. 2 Crystal structure of α–Fe2O3 |
1.2 计算方法
密度泛函论理采用量子力学方法研究多体系统的电子结构性质,利用电子密度ρ(r)取代电子波函数来描述和确定体系的基本量,将含有4N个变量的多粒子体系的薛定谔方程简化为3个空间变量的函数,大幅降低体系的自由度,使得理论计算成为可行[19]。随着计算机容量、运行速度和精度的不断提升,DFT方法的优势日趋明显,可以快速的基于物质的基本结构和性质,较为准确的模拟计算得到物质的化学反应特性及机理,建立物质的宏观物理和化学特性与其微观电子结构之间的关系,揭示化学反应的内在本质和规律[20]。
本文计算部分基于Materials Studio中的CASTEP模块,采用广义梯度近似(generalized gradient approximation,GGA)和Perdew–Burke–Ernzerhof(PBE)[21]的交互相关能对模型计算研究。电子波函数以平面波基组展开,离子实采用超软赝势描述,平面波截断能设置为Eout = 350 eV。表面的布里渊区(Brillouin zone)积分计算采用4×4×1的Monkhorst–Pack格点,自洽场(SCF)采用BFGS算法,迭代收敛精度为1×10–6 Ha,采用模型周期性边界条件。体系几何结构优化以位移、能量和力收敛为判据,其收敛阀值为1×10–6 Ha、最大位移0.000 5 nm和1×10–5 Ha,原子间力的最大值约小于0.002 Ha/nm时弛豫结束。所有反应的过渡态(transit state,TS)均采用线性同步转变(linear synchronous transit,LST)和二次同步转变(quadratic synchronous transit,QST)方法进行搜索[22]。
分子动力学模拟采用COMPASS力场,应用周期性边界条件,结合最速下降法和共轭梯度法,通过能量最小化来优化CO、Fe2O3(104)和Co–Fe2O3(104)体系的初始结构。采用NPT系统[23]研究CO在Fe2O3(104)和Co–Fe2O3(104)表面等温吸附过程,模拟时间步长为1,截断半径为10。PME方法用来计算长程静电相互作用[24]。
2 CO分子在Co掺杂Fe2O3模型表面上的吸附和反应 2.1 Co–Fe2O3层模型电子特性Qin等[25-26]通过形貌控制对氧化铁的高米勒指数表面(104)进行了实验和理论研究,发现其活性高于氧化铁自然裸露的主要表面(001)。因此研究了Co掺杂对Fe2O3(104)表面性能的改性作用。由于Fe2O3(104)表面的Fe原子存在3种不同的配位数(分别标记Fe5f、Fe6f和Fe7f),且有研究表明表面不同配位数原子在化学反应中具有不同的活性[27],因此以Co原子分别替换这3种Fe原子的方式对Fe2O3(104)表面进行了掺杂改性,并与纯净的Fe2O3(104)表面进行对比研究。结构优化后得到如图3的纯净Fe2O3(104)的稳定构型以及掺杂改性的Co5f–Fe2O3(104)、Co6f–Fe2O3(104)和Co7f–Fe2O3(104)的稳定构型。
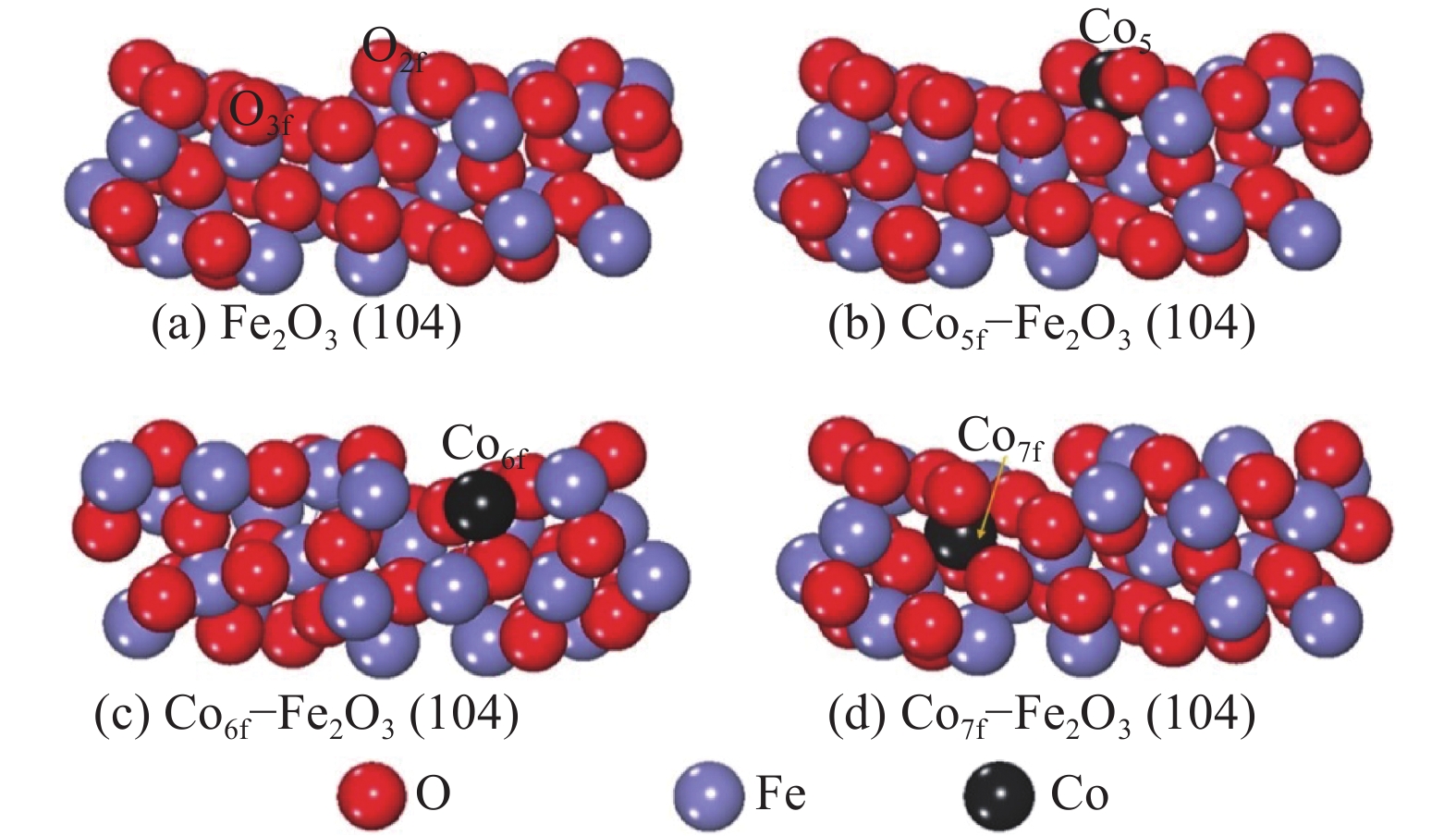 |
| 图3 Fe2O3(104)和Co–Fe2O3(104)的稳定构型 Fig. 3 Stable configuration of Fe2O3(104) and Co–Fe2O3(104) |
在化学链反应中,载氧体表面原子的成键参数、电子态密度以及表面能等参数决定了其反应活性。因此,可以通过对比这些参数的变化来评价Co掺杂对于Fe2O3表面电子结构改性能力。为分析Co在Fe2O3表面原子位点掺杂的难易程度,计算了Co掺杂后的结合能Ebind(eV):
| $ {E_{{\rm{bind}}}} \!=\! E({\rm{Co}} \!-\! {\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3})\!-\!(E({\rm{F}}{{\rm{e}}_2}{{\rm{O}}_3})\!-\!E\left( {{\rm{Fe}}} \right))\!-\!E\left( {{\rm{Co}}} \right) $ | (1) |
式中,E(Co–Fe2O3)为Co掺杂后体系的总能量,E(Fe2O3)为纯净Fe2O3体系的总能量,E(Fe)和E(Co)分别为Fe原子Co原子的总能量。
在CoO的晶体中,体相中的O与Co原子的配位数是6,Fe2O3体相中O与Fe原子的配位数是4,但其表面O原子的配位数为2和3,研究表明这些不同的配位数的O原子在化学反应中具有不同的反应特性[28]。因此,考虑了Co掺杂对表面的O原子成键的影响作用。表1列出了Co在Fe5f、Fe6f和Fe7f位掺杂的结合能以及Co掺杂位相邻O2f和O3f原子的平均键长(LO-M)(M代表Fe或Co)。Co在Fe5f和Fe6f位掺杂是放热过程,其中Co在配位数为5的Fe原子位掺杂时,放出的热量最大,且在7重配位Fe原子的掺杂属于是吸热反应。根据式(1),Co5f–Fe2O3(104)模型体系最为稳定,其次是Co6f–Fe2O3(104)模型掺杂。
| 表1 掺杂Co前后表面O的平均键长和掺杂Co的结合能 Tab. 1 Average bond length of O on the pure and Co-doped surfaces and the bind energy of Co-doped |
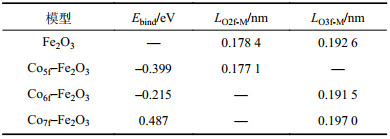 |
由图3和表1可知,Fe2O3(104)表面O2f和O3f存在悬键,O和Fe原子之间需要共用更多的电子紧密结合,使得表面张力降低键长变短,其平均键长小于体相中LO4f-Fe(0.196 0 nm)[29-30]。以Co原子替换Fe5f和Fe6f原子时,由于表面O原子的悬键增多,因此LO2f-M和LO3f-M平均键长均变短,而Co掺杂在Fe2O3(104)表面层的Fe7f位后,LO3f-M平均键长增加了0.004 4 nm,表明氧原子得到了一定程度的活化。这是因为掺杂位点Fe7f的配位数大于CoO晶体中6重配位的稳定结构,这种不匹配的晶格特征与掺杂的结合能Ebind结果一致,Co在Fe2O3(104)表面7重配位的Fe原子的掺杂结合能为正值,表明需要外加能量才可以进行掺杂。
Co掺杂后体系表面的态密度发生了变化,其中Co7f–Fe2O3(104)的态密度图显示在3 eV能量附近有一个明显的突起小峰,如图4所示。此外,纯净模型和掺杂模型的态密度在–10~–8 eV能量范围均有较强的定域,而在–8~0 eV能量范围内电子离域作用较强,与之前的Co掺杂铁基载氧体与褐煤的实验研究结果一致[31]。而且Co5f–Fe2O3(104)模型体系靠近费米能级左边的填充态能量稍微高于其他模型。
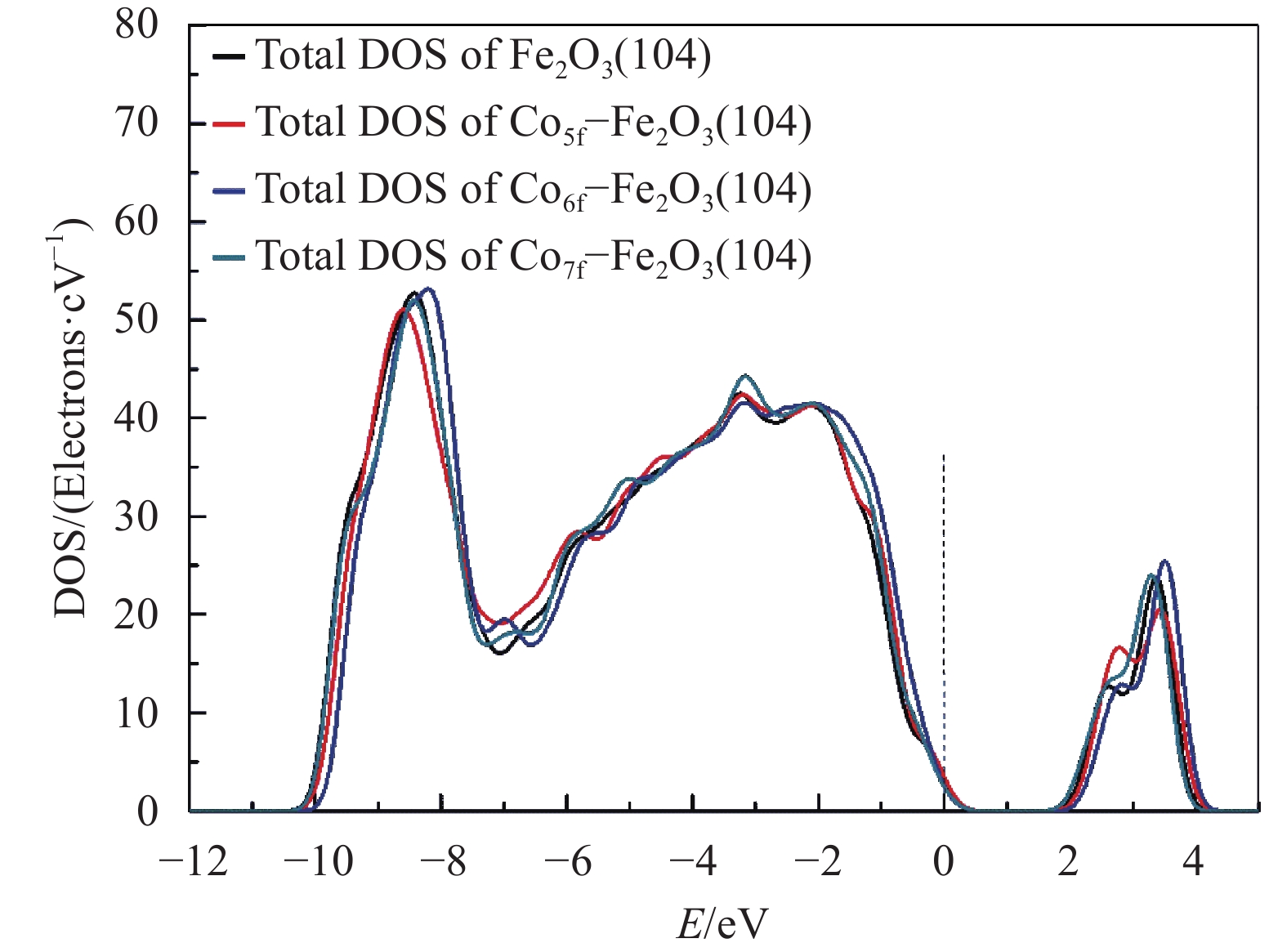 |
| 图4 Fe2O3(104)、Co5f–Fe2O3(104)、Co6f–Fe2O3(104)和Co7f–Fe2O3(104)的总态密度 Fig. 4 Total density of state (DOS) of Fe2O3(104), Co5f–Fe2O3(104), Co6f–Fe2O3(104) and Co7f–Fe2O3(104) |
2.2 CO在Co–Fe2O3层模型表面的吸附
图5(a)为800 ℃下CO在Fe2O3(104)和Co掺杂的Fe2O3(104)表面的等温吸附线,表示了CO分子在不同逸度下的吸附量。从图5(a)可以看出,相同逸度下CO在Co5f–Fe2O3(104)的吸附量稍微多一点,而在Co7f–Fe2O3(104)的吸附量最少,低于CO在纯净的Fe2O3表面的吸附量,表明Co7f–Fe2O3(104)吸附CO的能力最弱。此外,CO在所有模型的等温吸附都属于Langmuir类型,符合下列的形式:
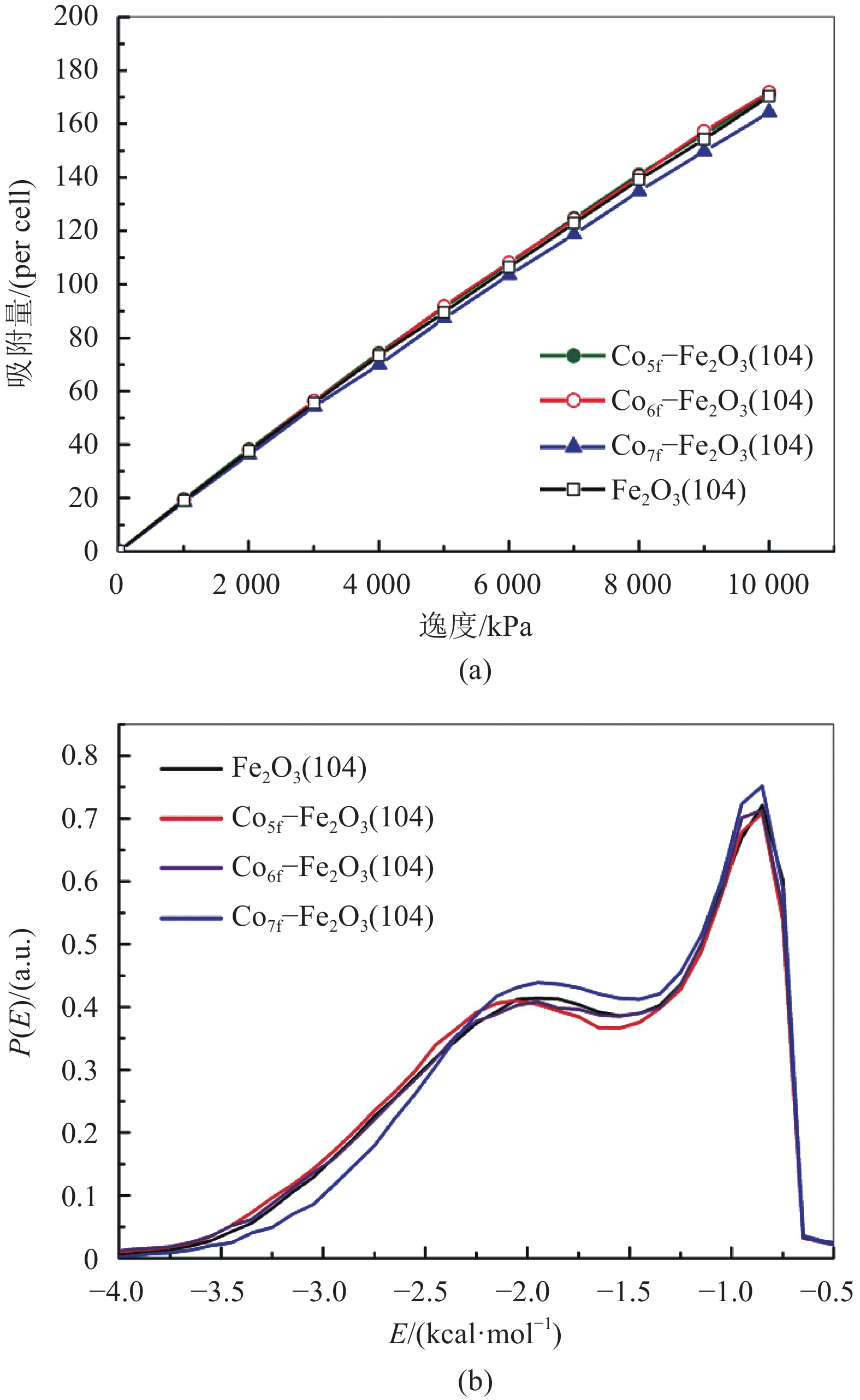 |
| 图5 800 °C下CO在Fe2O3(104)和Co掺杂的Fe2O3(104)的等温吸附和体系的能量分布函数 Fig. 5 Adsorption isotherms and energy distribution functions for CO/Co–Fe2O3(104) interaction systems at 800 °C |
| ${\theta _{\rm{t}}} = \frac{{{{(K'c)}^\eta }}}{{{{\left[ {1 + (K'c)} \right]}^{\eta /k}}}}$ | (2) |
式中:
| $ {\varGamma _t}(p,{T} ) = \int {\varGamma (p,{T} ,U)f(U){\rm d}U} $ | (3) |
式中,Гt为总的等温吸附,Г为局部等温吸附,f (U)为能量分布函数,T为800 ℃。
根据以上CO的等温吸附分析,Langmuir局部等温吸附模型可以很好地描述能量分布的不均匀性。图5(b)为800 ℃下CO在Fe2O3和Co掺杂Fe2O3表面吸附能量分布曲线,从图中可以出,CO在Fe2O3(104)和Co掺杂Fe2O3(104)表面的吸附存在两种方式,–2.0 eV附近的峰为CO模型表面碱性位点的吸附,–0.75 eV附近的峰为CO在非碱性位点的吸附。CO在Co5f–Fe2O3(104)表面的吸附作用比在Co6f–Fe2O3(104)和Co7f–Fe2O3(104)表面的吸附作用强。
为研究掺杂模型表面Co对表面结构和性能的影响,以一个CO分子靠近Co原子构建吸附模型,由于Co掺杂后相邻的O原子有O2f或O3f两种配位结构,因此建立了如图6所示的稳定吸附模型:(a)Fe2O3(104)–O2f、(b)Fe2O3(104)–O3f、(c)Co5f–Fe2O3(104)–O2f、(d)Co6f–Fe2O3(104)–O3f和(e)Co7f–Fe2O3(104)–O3f。计算得到了吸附后CO在纯净表面和掺杂表面的吸附能(Eads)、C–O键长(LCO)以及与表面的吸附位的距离(Dsur)和形成的夹角(Asur)等参数,见表2。
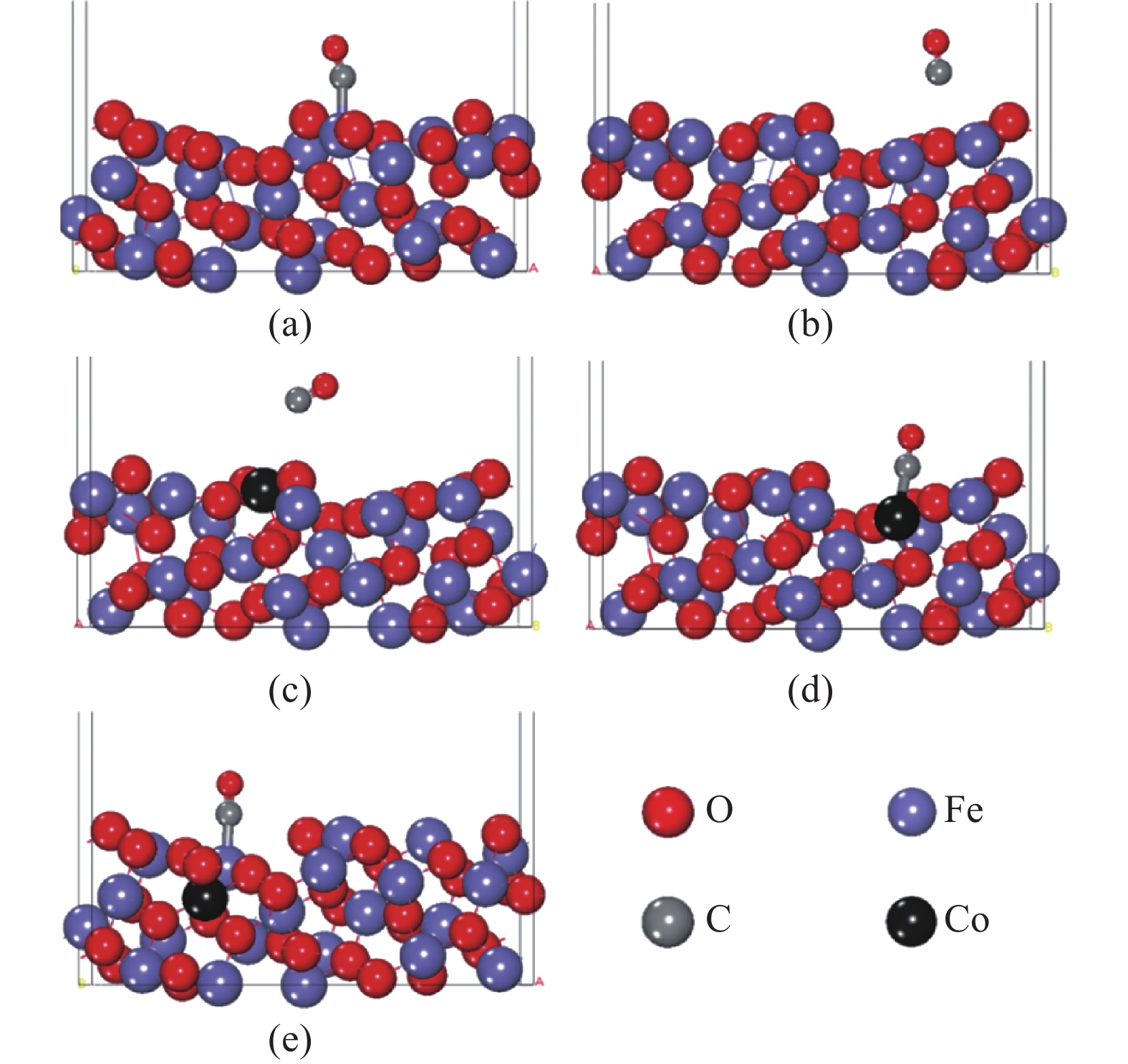 |
| 图6 CO在Fe2O3(104)及Co掺杂表面的稳定吸附构型 Fig. 6 Stable configurations of CO absorbed on Fe2O3(104) and Co-doped surfaces |
| 表2 CO在表面稳定吸附后的键长(LCO)以及与表面的吸附位的距离(Dsur)、夹角(Asur)和吸附能(Eads) Tab. 2 Bond length (LCO) of CO and its distance (Dsur) and angle (Asur) adsorption energy (Eads) with the adsorbed site after adsorbing on surfaces |
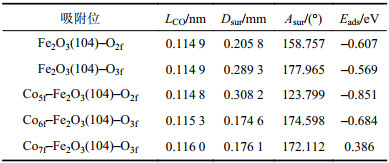 |
CO分子在Fe2O3(104)表面O2f和O3f位点附近吸附后的键结构活化程度变化均不明显,而在Co6f和Co7f掺杂的表面的O2f或O3f位点吸附时,CO的C–O键长分别增加了0.000 4和0.001 1 nm,表明Co掺杂表面对CO分子的活化作用较大。吸附能数据显示CO分子在Fe2O3(104)、Co5f–Fe2O3(104)和Co6f–Fe2O3(104)3个表面上的吸附反应均为放热过程,而在Co7f–Fe2O3(104)表面吸附为吸热过程,说明高温下CO分子更容易在Co7f–Fe2O3(104)表面吸附。
2.3 CO在Co–Fe2O3层模型表面的反应CO的化学链燃烧过程为气–固接触反应,需经过吸附、氧化和解离3个阶段[32]。因此,模拟计算反应过程如下:CO首先从无穷远处接近Fe2O3并形成吸附,其次与表面Fe和O原子作用形成OCO结构,最后脱离表面形成CO2。以CO分子在纯净模型和掺杂模型表面的O2f或O3f位点附近稳定结构为始态(initial state,IS),以CO2分子在模型表面的生成为终态(final state,FS)利用LST/QST方法进行过渡态搜索,得到相应的过渡态(TS)、反应活化能和反应路径。
图7为CO与Fe2O3(104)表面反应生成CO2的反应路径。图7(a)中CO吸附过程中与表面Fe原子成键,形成稳定吸附,而图7(b)中CO与表面没有成键,与表2中CO到表面的距离Dsur结果一致。图7(a)和(b)中的过渡态结构有明显的不同,前者CO与表面O2f结合OCO产物并吸附在表面,而后者中O3f在CO作用下形成了游离的O离子,结合能量变化可知CO与O3f原子结合生成CO2的反应活化能较高。此外,CO与Fe2O3(104)表面O2f和O3f位作用生成CO2的反应均为放热过程,释放的能量分别1.048和1.648 eV。结果表明CO在Fe2O3(104)表面O2f位点的氧化反应更容易进行,与CO在O2f和O3f位点吸附过程中的被活性程度一致。
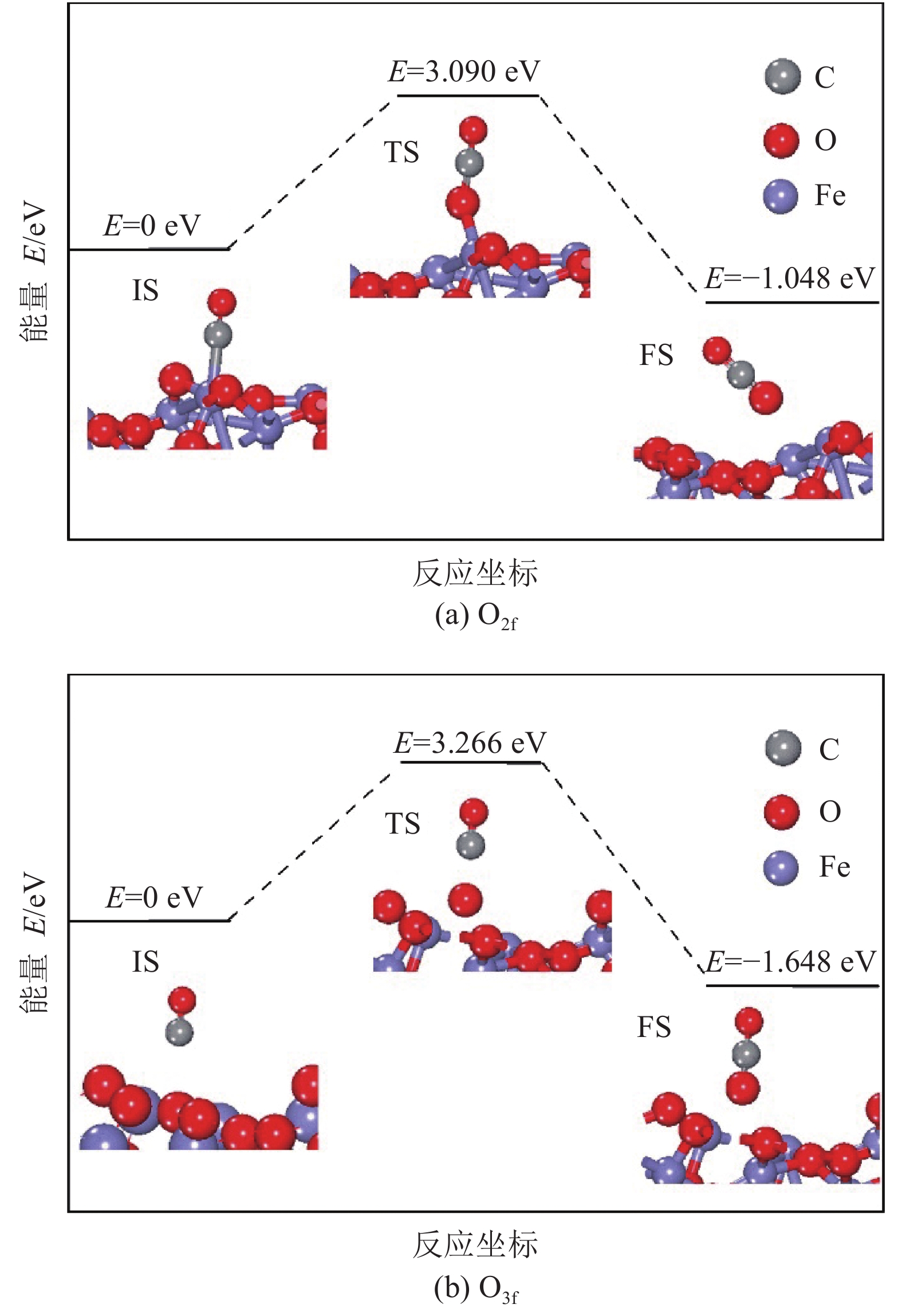 |
| 图7 CO在Fe2O3(104)的O2f和O3f位点氧化生成CO2的能量变化曲线 Fig. 7 Calculated potential energy profiles for CO oxidation on O2f and O3f of Fe2O3(104) |
CO在Co5f–Fe2O3(104)模型表面的Co原子作用时向相邻的O原子(O2f)方向移动,最终形成稳定吸附构型,如图8所示。过渡态结构显示O2f向CO靠近但没有形成化学键,分析原因是CO在该模型表面吸附位置与表面距离较大(Dsur=0.308 2 nm),分子间的范德华力(van der Waals force)较低。但反应生成CO2所需的活化能(2.572 eV)低于CO在Fe2O3(104)表面生成CO2的活化能(3.090 eV),且相应的反应能增加了0.445 eV。表明Co在Fe5f位的掺杂不仅提高了Fe2O3表面的反应活性,而且可以释放出更多的能量。
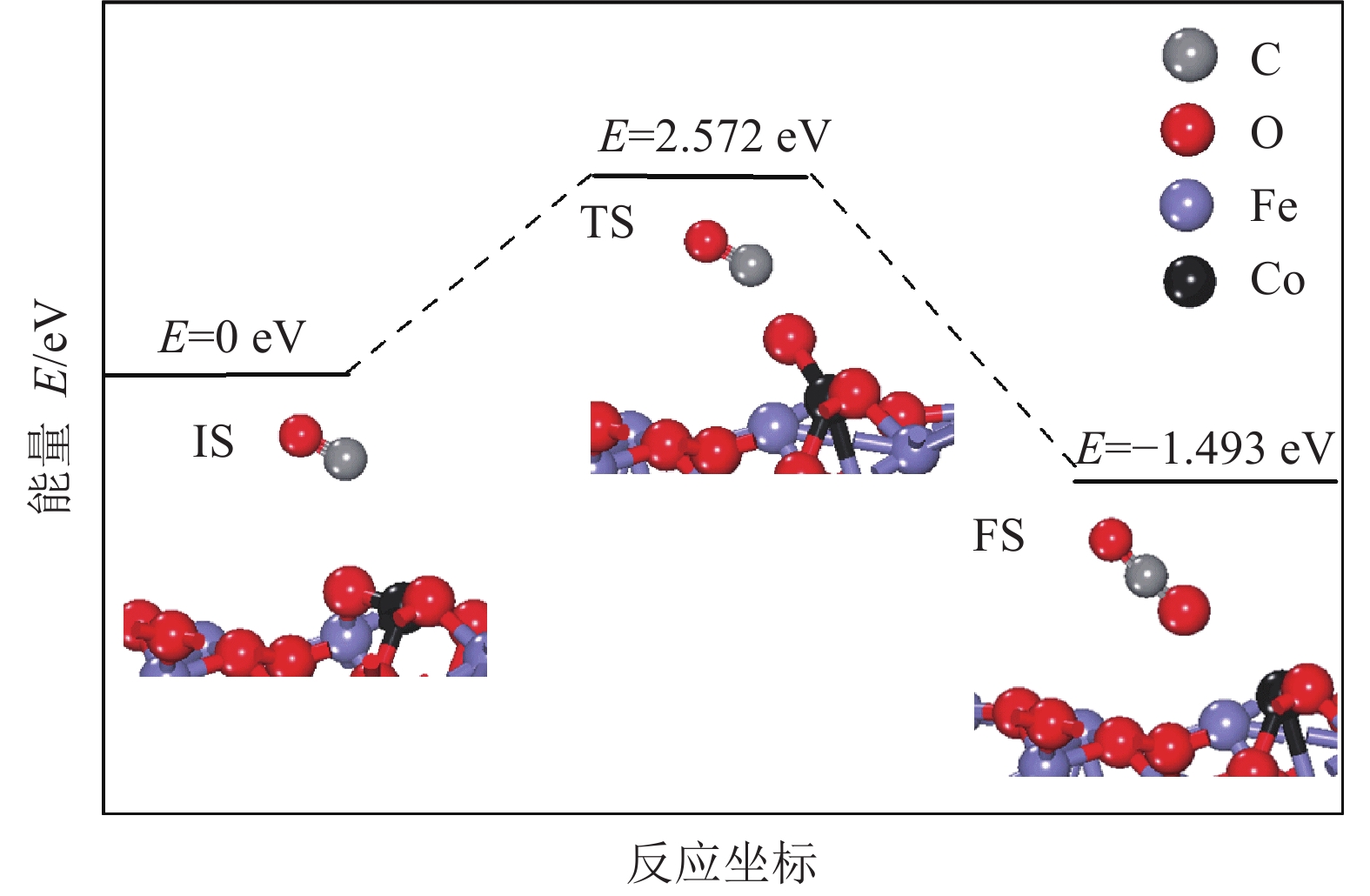 |
| 图8 CO与O2f作用还原Co5f–Fe2O3(104)表面的反应路径能量变化曲线 Fig. 8 Potential energy profiles of CO with O2f on the Co5f–Fe2O3(104) surface |
图9(a)、(b)分别是Co6f–Fe2O3(104)和Co7f–Fe2O3(104)表面的O3f原子与CO分子作用生成CO2的反应路径。图9(a)过渡态结构与始态相近,CO以C端吸附在Co原子上,O3f原子向CO靠近,生成CO2的反应活化能较Fe2O3(104)表面O2f位高出了0.079 eV,但仍低于其O3f位反应活化能,反应过程为放热反应,放出的热量则减少了0.151 eV。图9(b)中过渡态为OCO结构,其生成CO2的反应活化能比在Fe2O3(104)表面与O3f位的活化能低0.285 eV,反应释放的能量则减少了0.388 eV。
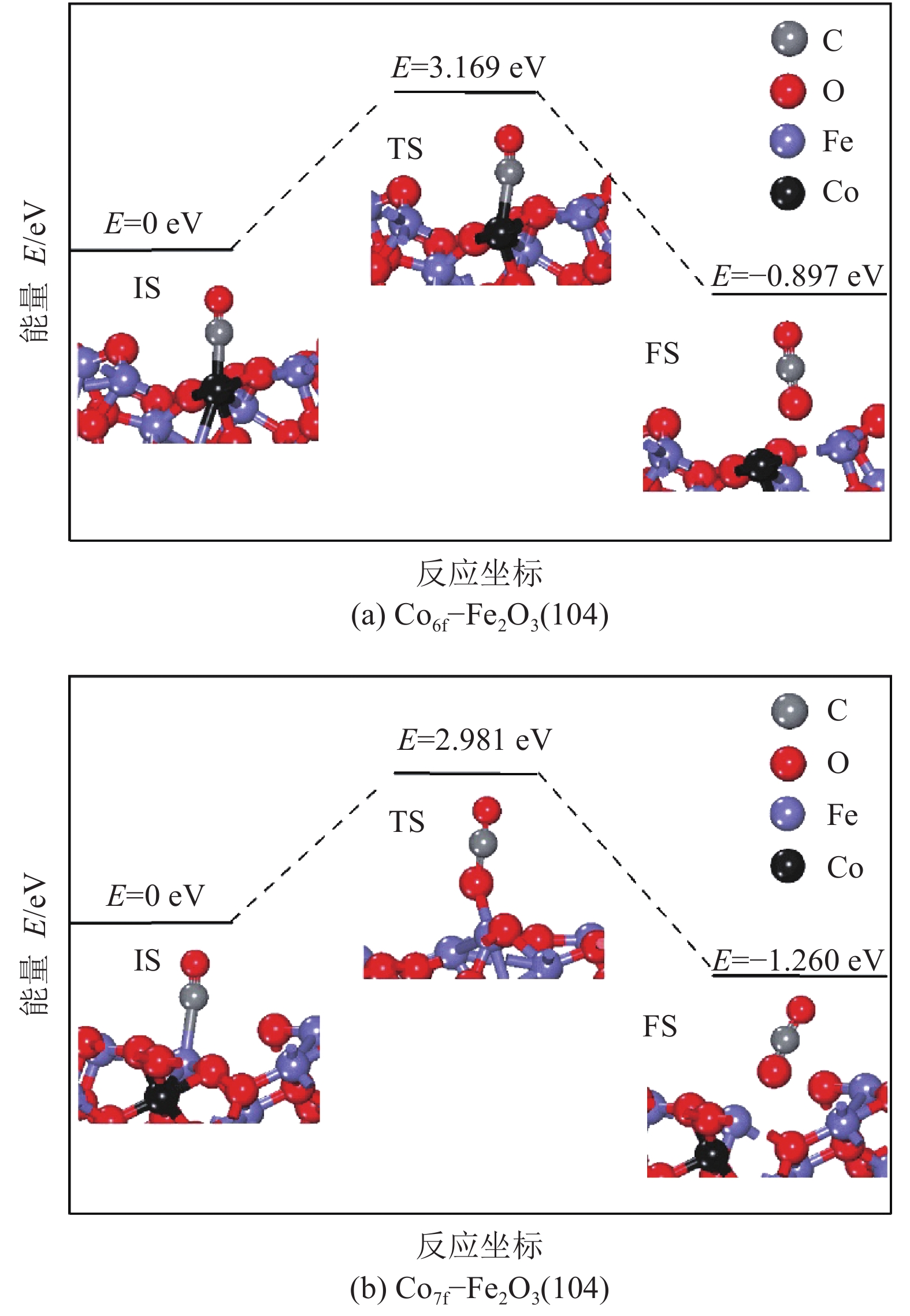 |
| 图9 CO与O3f作用还原Co6f–Fe2O3(104)表面和Co7f–Fe2O3(104)表面的反应路径能量变化曲线 Fig. 9 Potential energy profiles of CO with O3f on the Co6f–Fe2O3(104) and Co7f–Fe2O3(104) surfaces |
综上结果表明,Co在Fe2O3(104)表面不同配位数Fe原子位掺杂对表面活性影响程度不同,但均能起到提高反应活性,降低氧化CO生成CO2的反应能垒。尽管CO在Co6f–Fe2O3(104)和Co7f–Fe2O3(104)表面反应生成CO2所释放的能量有一定的减少,但Co掺杂有助于提高铁基载氧体的反应活性,对于提高化学链燃烧反应的效率有显著的影响。
3 结 论Co掺杂改性有助于提高Fe2O3(104)表面的反应活性,降低氧化CO的反应能垒。具体作用如下:Co掺杂增大了体系的总态密度在–8 eV到0 eV范围内的离域性,活化表面掺杂点相邻的O原子,促使O原子平均键长增加,从而易于脱离表面与燃料结合。CO的等温吸附结果表明,Co5f–Fe2O3(104)和Co5f–Fe2O3(104)表面吸附CO分子量增加,且CO分子的C–O键长不同程度的增长,其中CO吸附在Co7f–Fe2O3(104)表面时C–O键最长,表明Co掺杂提高了CO在Fe2O3(104)表面的吸附量和活化程度。反应路径和过渡态分析表明,Co掺杂降低了表面氧化CO生成CO2的反应活化能,并且在Fe5f位掺杂Co原子反应活化能最低。综上表明Co掺杂能够提高铁基载氧体的反应活性,因此下一步的研究将围绕改性铁基载氧体的金属成分、掺杂比例和方式等方面展开研究,为化学链中载氧体的开发和优化提供一定的理论基础。
| [1] |
Richter H J,Knoche K F.Reversibility of combustion processes,efficiency and costing,second law analysis of processes[C]//American Chemical Society Symposium Series 1983.Washington D C:ACS,1983:71–85.
|
| [2] |
Jin H T,Ishida M. Development of a novel chemical-looping combustion:Synthesis of a solid looping material of NiO/NiAl2O4[J]. Industrial & Engineering Chemistry Research, 1998, 38(1): 126-132. DOI:10.1021/ie9803265 |
| [3] |
Matzen M,Pinkerton J,Wang Xiaomeng,et al. Use of natural ores as oxygen carriers in chemical looping combustion:A review[J]. International Journal of Greenhouse Gas Control, 2017, 65: 1-14. DOI:10.1016/j.ijggc.2017.08.008 |
| [4] |
Wang P N.Means D S,et al. Chemical-looping combustion and gasification of coals and oxygen carrier development:A brief review[J]. Energies, 2015, 8(10): 10605-10635. DOI:10.3390/en81010605 |
| [5] |
Blas L,Dorge S,Michelin L,et al. Influence of the regeneration conditions on the performances and the microstructure modifications of NiO/NiAl2O4 for chemical looping combustion
[J]. Fuel, 2015, 153: 284-293. DOI:10.1016/j.fuel.2015.03.015 |
| [6] |
Liang Zhiyong,Dong Changqing,Qin Wu,et al. Review on optimization of iron based oxygen carriers in chemical-looping combustion[J]. Modern Chemical Industry, 2017, 37(2): 36-40. [梁志永,董长青,覃吴,等. 化学链燃烧中铁基载氧体性能优化研究综述[J]. 现代化工, 2017, 37(2): 36-40.] |
| [7] |
Kang Dohyung,Hyun S L,Lee Minbeom,et al. Syngas production on a Ni-enhanced Fe2O3/Al2O3 oxygen carrier via chemical looping partial oxidation with dry reforming of methane
[J]. Applied Energy, 2018, 211: 174-186. DOI:10.1016/j.apenergy.2017.11.018 |
| [8] |
Li Qu,Qin Wu,Zhang Junjiao,et al. Characteristics and kinetics of chemical looping combustion of Mn-doped Fe2O3 oxygen carrier with CO
[J]. Journal of Fuel Chemistry and Technology, 2014, 42(8): 932-937. [李渠,覃吴,张俊姣,等. Mn-Fe2O3载氧体作用下CO化学链燃烧特性及动力学研究
[J]. 燃料化学学报, 2014, 42(8): 932-937. DOI:10.3969/j.issn.0253-2409.2014.08.005] |
| [9] |
Jiang Bo,Li Lin,Bian Zhoufeng,et al. Hydrogen generation from chemical looping reforming of glycerol by Ce-doped nickel phyllosilicate nanotube oxygen carriers[J]. Fuel, 2018, 222: 185-192. DOI:10.1016/j.fuel.2018.02.096 |
| [10] |
Miller D D,Siriwardane R. Mechanism of methane chemical looping combustion with hematite promoted with CeO2[J]. Energy & Fuels, 2013, 27(8): 4087-4096. DOI:10.1021/ef302132e |
| [11] |
Gu Haiming,Shen Laihong,Xiao Jun,et al. Cycle experiments on chemical looping combustion of coal using potassium-improved iron ore as oxygen carrier[J]. Journal of Fuel Chemistry and Technology, 2012, 40(8): 33-40. [顾海明,沈来宏,肖军,等. 基于钾基修饰铁矿石载氧体的煤化学链燃烧循环实验[J]. 燃料化学学报, 2012, 40(8): 33-40.] |
| [12] |
Zhang Siwen,Shen Laihong,Xiao Jun,et al. Catalytic combution of coal using alkali and transition metals loaded on iron ore oxygen carrier[J]. Journal of Fuel Chemistry and Technology, 2012, 40(10): 1179-1187. [张思文,沈来宏,肖军,等. 基于碱金属和过渡金属修饰铁矿石载氧体的煤催化燃烧[J]. 燃料化学学报, 2012, 40(10): 1179-1187. DOI:10.3969/j.issn.0253-2409.2012.10.005] |
| [13] |
Hossain M M,de Lasa H I. Reduction and oxidation kinetics of Co-Ni/Al2O3 oxygen carrier involved in a chemical-looping combustion cycles
[J]. Chemical Engineering Science, 2010, 65(1): 98-106. DOI:10.1016/j.ces.2009.01.059 |
| [14] |
Qin Wu,Li Qu,Dong Changqing,et al. CO chemical looping combution using Co–Fe2O3 nano oxygen carrier for enrichment of CO2[J]. CIESC Journal, 2014, 65(8): 3136-3143. [覃吴,李渠,董长青,等. Co-Fe2O3纳米载氧体作用下CO化学链燃烧富集CO2[J]. 化工学报, 2014, 65(8): 3136-3143. DOI:10.3969/j.issn.0438-1157.2014.08.039] |
| [15] |
Qin Wu,Hou Cuicui,Zhang Junjiao,et al. Chemical looping combution characteristics of Lignite using Co–Fe2O3(104)/Al2O3 oxygen carrier
[J]. CIESC Journal, 2016, 67(4): 1459-1466. [覃吴,侯翠翠,张俊姣,等. Co–Fe2O3(104)铁基载氧体优化体系作用下褐煤化学链燃烧特性
[J]. 化工学报, 2016, 67(4): 1459-1466.] |
| [16] |
Bhavsar S,Natalie I,Amey M,et al. Lanthana-doped ceria as active support for oxygen carriers in chemical looping combustion[J]. Applied Energy, 2016, 168: 236-247. DOI:10.1016/j.apenergy.2016.01.073 |
| [17] |
Rollmann G,Rohrbach A,Entel P,et al. First-principles calculation of the structure and magnetic phases of hematite[J]. Physical Review (B), 2004, 69(16): 1-12. DOI:10.1103/PhysRevB.69.165107 |
| [18] |
Sandratskii L M,Uhl M,Kübler J. Band theory for electronic and magnetic properties of α–Fe2O3[J]. Journal of Physics:Condensed Matter, 1996, 8(8): 983-989. DOI:10.1088/0953-8984/8/8/009 |
| [19] |
Meng Qiangqiang.First-principles study of electronic properties of several metal oxides[D].Hefei:University of Science and Technology of China,2014. 孟强强.若干金属氧化物电子结构的第一性原理研究[D].合肥:中国科学技术大学,2014. |
| [20] |
Liang Zhiyong.Study on the mechanism of deep oxidation of CO and carbon formation on iron-based oxygen carrier[D].Beijing:North China Electric Power University,2017. 梁志永.铁基载氧体深层氧化CO以及积碳形成机理研究[D].北京:华北电力大学,2017. |
| [21] |
Ling L,Song J,Zhao S,et al. DFT study on the effects of defect and metal-doping on the decomposition of H2S on the α–Fe2O3(0001) surface
[J]. RSC Advances, 2014, 4(43): 22411. DOI:10.1039/c4ra02485k |
| [22] |
Zhang X,Song X,Sun Z,et al. Density functional theory study on the mechanism of calcium sulfate reductive decomposition by carbon monoxide[J]. Industrial & Engineering Chemistry Research, 2012, 51(18): 6563-6570. DOI:10.1021/ie202203b |
| [23] |
Phillips J C,Braun R,Wang W,et al. Scalable molecular dynamics with NAMD[J]. Journal Computional Chemstry, 2005, 26(16): 1781-1802. DOI:10.1002/jcc.20289 |
| [24] |
Darden T,York D,Pedersen L. Particle mesh Ewald:An N·log(N) method for Ewald sums in large systems[J]. The Journal of Chemical Physics, 1993, 98(12): 10089-10092. DOI:10.1063/1.464397 |
| [25] |
Qin W,Wang Y,Lin C,et al. Possibility of morphological control to improve the activity of oxygen carriers for chemical looping combustion[J]. Energy & Fuels, 2015, 29(2): 1210-1218. DOI:10.1021/ef5024934 |
| [26] |
Qin Wu,Lin Changfeng,Long Dongteng,et al. Reaction activity and deep reduction reaction mechanism of a high index iron oxide surface in chemical looping combution[J]. Acta Physico-Chimica Sinica, 2015, 31(4): 667-675. DOI:10.3866/pku.whxb201502061 |
| [27] |
Qin W,Wang Y,Dong C,et al. The synergetic effect of metal oxide support on Fe2O3 for chemical looping combustion:A theoretical study
[J]. Applied Surface Science, 2013, 282: 718-723. DOI:10.1016/j.apsusc.2013.06.041 |
| [28] |
Liang Zhiyong,Wang Jianye,Qin Wu,et al. Theoretical analysis of the CO reaction mechanism on Fe2O3(1-12) surface during chemical looping combustion
[J]. Acta Scientiae Circumstantiae, 2017, 37(5): 1826-1834. [梁志永,王建业,覃吴,等. Fe2O3(1-12)作用下CO化学链燃烧反应机理研究
[J]. 环境科学学报, 2017, 37(5): 1826-1834. DOI:10.3321/j.issn:1672-2043.2008.05.024] |
| [29] |
Yang T,Wen X,Ren J,et al. Surface structures of Fe3O4(111),(110),and (001):A density functional theory study
[J]. Journal of Fuel Chemistry and Technology, 2010, 38(1): 121-128. DOI:10.1016/s1872-5813(10)60024-2 |
| [30] |
Lo C,Tanwar K,Chaka A,et al. Density functional theory study of the clean and hydrated hematite (1
|
| [31] |
Youmbi B S,Calvayrac F. Structure of CoO(001) surface from DET+U calculations[J]. Surface Science, 2014, 621: 1-6. DOI:10.1016/j.susc.2013.10.012 |
| [32] |
Liang Zhiyong,Wu Qin,Dong Changqing. Experimental and theoretical study of the interactions between Fe2O3/Al2O3 and CO
[J]. Energies, 2017, 10(5): 598-612. DOI:10.3390/en10050598 |
 2019, Vol. 51
2019, Vol. 51


