2. 河南恒安环保科技有限公司,河南 郑州 450001;
3. 扬州大学 环境科学与工程学院,江苏 扬州 225127
2. Henan Hengan Environmental Protection Technol. Co., Ltd., Zhengzhou 450001, China;
3. College of Enviromental Sci. and Eng., Yangzhou Univ., Yangzhou 225127, China
20世纪末纳米材料已经广泛用于人类的生产和生活,如乳化剂、催化剂、半导体、化妆品等均涉及纳米材料[1]。纳米ZnO(Nano–ZnO)和纳米CuO(Nano–CuO)具有特殊的光学、催化和半导体特性,使其在催化、化妆品、油漆等方面广泛使用,且Nano–ZnO以每年528 t的生产速度持续增长[2]。由于管道泄漏、磨损以及人为等因素,使部分Nano–ZnO和Nano–CuO颗粒流入环境并且逐渐积累,泄露的纳米颗粒通过水利管道进入城市污水处理厂。部分污水处理厂中Nano–ZnO浓度已达到1 mg/L,且不断增加[3]。研究发现,10 mg/L Nano–ZnO能够显著抑制硝化菌活性[3],Nano–CuO的积累对短程硝化[4]、厌氧氨氧化[5]等脱氮系统具有显著影响。污水处理系统以吸附污泥方式截留98%以上的纳米颗粒。可见,随着纳米材料的使用,污水处理厂污泥中富集的纳米颗粒浓度将会越来越高,对于污泥处理、污水处理均具有不可忽视的影响[6]。
随着对污泥处理的重视,污泥资源化和无害化得到广泛研究。污泥厌氧发酵是目前应用最广泛的污泥处理技术。研究发现Nano–ZnO和Nano–CuO对细菌等具有毒性作用[7]。Mu等[8]发现150 mg/g TSS(Nano–ZnO)对污泥具有显著抑制作用。同时,大多数研究中污泥有机质比(MLVSS/MLSS)为0.6~0.8[9]。由于部分城市排水管网仍采用雨污合流,使进入污水处理厂的无机物含量增大,剩余污泥有机质含量降低。29个城市污水处理厂调查发现,大多数污水处理厂剩余污泥有机质比的平均值为0.384[10]。目前,Liao等[11]将MLVSS/MLSS ≤ 0.5定义为低有机质污泥。孙通等[12]研究发现:有机质比为0.256的污泥厌氧消化甲烷产量为160.29 mg/g VSS,有机质比为0.5的甲烷产量为809.33 mg/g VSS,可见,低有机质污泥热值较低,其消化处理难度大,处理成本升高。富含纳米颗粒的低有机质剩余污泥处置将更为艰难。因此,研究Nano–ZnO和Nano–CuO对低有机质剩余污泥厌氧发酵性能的影响是必要的。
作者将低有机质剩余污泥在Nano–ZnO和Nano–CuO条件下进行厌氧发酵处理。通过分析不同发酵系统中的SCFAs、蛋白质、多糖、蛋白酶、α–葡萄糖苷酶、碱性磷酸酶、酸性磷酸酶、脱氢酶、功能微生物等指标,探讨Nano–ZnO和Nano–CuO对低有机质剩余污泥厌氧发酵性能的影响。研究Nano–ZnO和Nano–CuO对污泥厌氧发酵的作用机制,
1 材料与方法 1.1 污泥来源及实验装置实验使用的污泥来自郑州市某城市污水处理厂二沉池回流污泥,使用前将其用自来水清洗3次进行浓缩,污泥性质如表1所示。
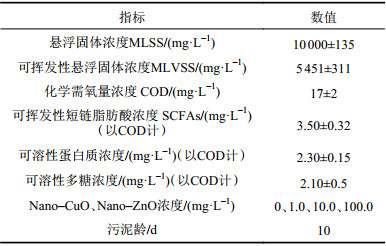
| 表1 实验污泥性质及运行模式 Tab. 1 Characteristic of test sludge and operation mode |
 |
Nano–ZnO和Nano–CuO来自上海阿拉丁生化科技股份有限公司,粒径均为小于100 nm。
实验反应器材料为有机玻璃,总体积为2.5 L,有效容积为2.0 L,采用磁力搅拌器进行匀速搅拌,转速为700 r/min,反应温度为室温。
1.2 试验方法剩余污泥首先利用自来水进行清洗浓缩至实验污泥浓度,分别取2 L实验污泥投加至1#~8#厌氧发酵反应器,分别向1#~4#厌氧发酵反应器中投加到Nano–CuO,控制浓度为0、1、10、100 mg/L,向5#~8#厌氧发酵反应器中投加Nano–ZnO,控制浓度为0、1、10、100 mg/L。启动磁力搅拌器,隔天取样测定理化指标。
1.3 分析方法 1.3.1 液体指标分析取适当体积发酵产物,采用8 000 r/min离心10 min,采用0.5 μm玻璃纤维膜抽滤上清液,抽滤液用于分析SCOD、蛋白质、多糖、
SCOD、
为了考察不同纳米颗粒对发酵系统中微生物种群的影响,在发酵末期分别取8个发酵系统发酵污泥利用Illumina MiSeq测序平台进行高通量测序。PCR引物:
341F/805R(341F:CCTACGGGNGGCWGCAG、805R:GACTACHVGGGTATCTAATCC)。
2 结果与讨论 2.1 污泥水解酸化性能蛋白质和多糖是污泥胞外聚合物(EPS)的重要组成部分,约为80%左右,同时也是污泥厌氧发酵系统中酸化菌的重要作用基质,不同发酵系统中蛋白质等浓度如表2、3所示。
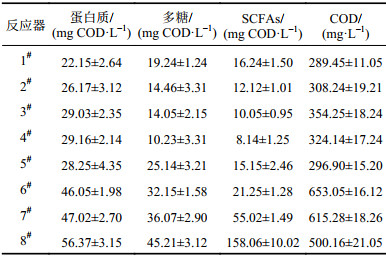
| 表2 不同发酵系统中蛋白质、多糖、SCFAs及COD浓度 Tab. 2 Production of soluble protein,soluble polysaccharide,SCFAs and COD in the different fermentation systems |
 |
| 表3 不同发酵系统中NH4 +–N、PO4 3––P和DNA浓度 Tab. 3 Production of NH4 +–N,PO4 3––P and DNA in the different fermentation systems |
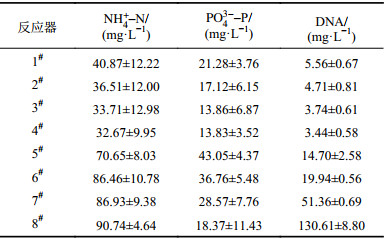 |
分析表2可知:不同浓度Nano–ZnO和Nano–CuO污泥厌氧发酵系统中,蛋白质、多糖、SCFAs和COD的产量具有显著差别,其中Nano–CuO发酵系统中蛋白质随着其增加而少量增大,分别为22.15、26.17、29.03和29.16 mg COD/L,但是多糖和SCFAs产量随着Nano–CuO投加量增加而降低,分别为19.24、14.46、14.05和10.23 mg COD/L(多糖),16.24、12.12、10.05和8.14 mg COD/L(SCFAs)。蛋白质、多糖和SCFAs产量随着Nano–ZnO投加量增加而增大,Nano–ZnO 4个发酵系统中,蛋白质、多糖和SCFAs的产量最大,分别为56.37、45.21及158.06 mg COD/L。说明Nano–ZnO能够促进厌氧发酵过程中低有机质污泥细胞壁溶解、有机质的释放,不同发酵系统中SCOD的产量也证实其作用,如表3中DNA所示,随着Nano–ZnO的投加量增加,DNA释放量提高。
Nano–ZnO发酵系统中蛋白质、多糖及SCFAs的产量远高于Nano–CuO发酵系统,其产量约为Nano–CuO发酵系统蛋白质产量的1.75~1.93倍、多糖产量的2.22~4.42倍、SCFAs产量的1.75~19.42倍,说明Nano–ZnO对低有机质剩余污泥厌氧发酵性能作用高于Nano–CuO。分析原因:Nano–CuO和Nano–ZnO在吸收光子后可以自发产生活性氧,在光照条件下光子吸收并扩散至Nano–CuO表面,激发电子形成超氧离子,或者在光照条件下电子空穴扩散至Nano–ZnO表面并与水形成羟基自由基,但是由于低有机质污泥厌氧发酵系统中属于厌氧状态没有溶解氧,所以Nano–CuO不能形成氧损伤,但是Nano–ZnO发酵系统能够产生具有氧化性的羟基自由基,这就导致其对污泥的水解性能不同。Zhang[16]等也证实,Nano–ZnO能够增加蛋白质水解,进而提高SCFAs积累。同时,pH值也可能是造成Nano–CuO和Nano–ZnO污泥厌氧发酵系统水解酸化性能不同的原因之一,如图1所示。
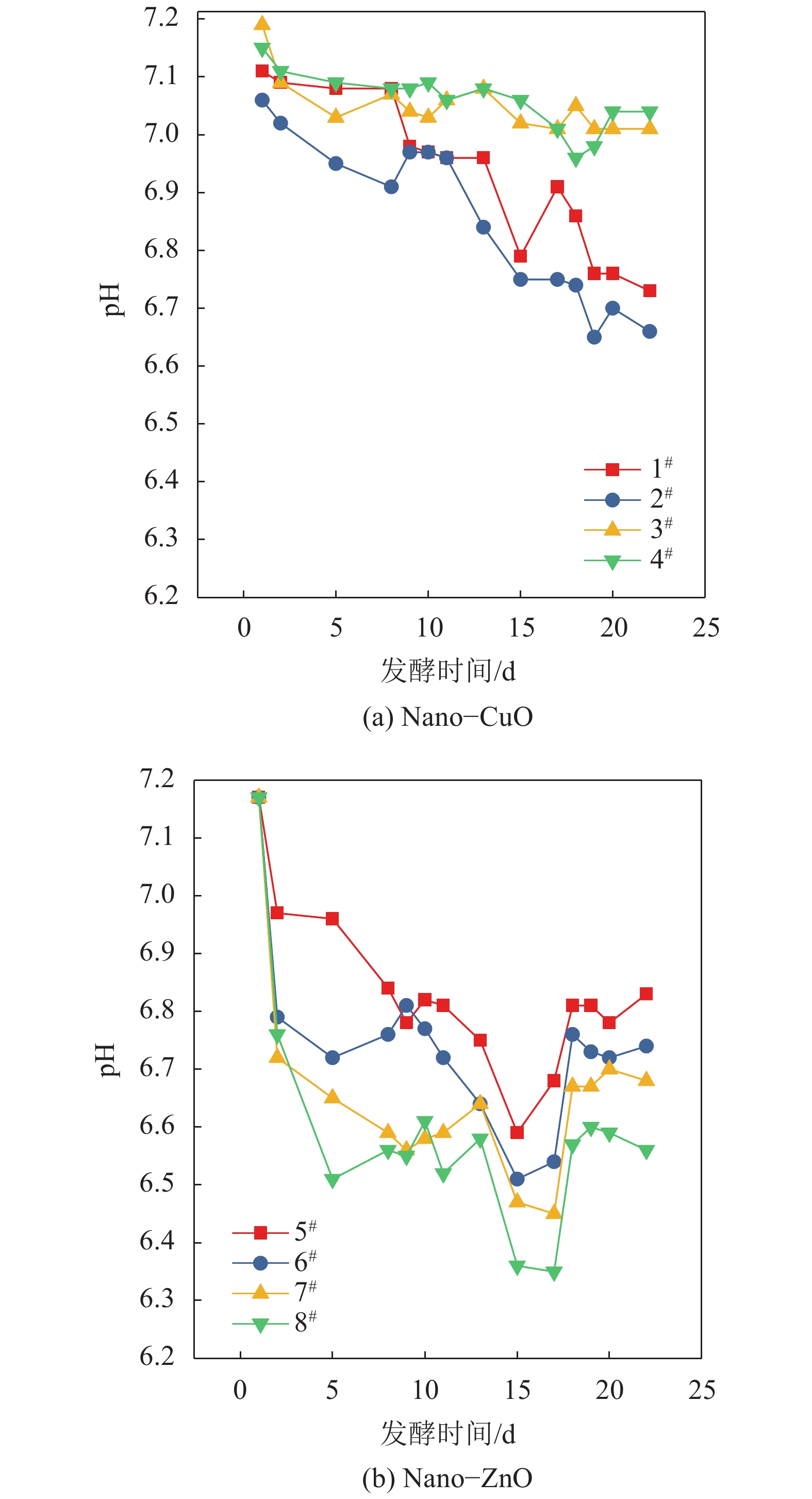 |
| 图1 pH值对厌氧发酵系统的影响 Fig. 1 Effect of pH values on anaerobic fermentation system |
Nano–ZnO 8#发酵系统中pH值为6.5,而Nano–CuO 4#发酵系统pH值为7.1,产甲烷菌最佳生长pH值为7,所以Nano–CuO发酵系统更适合产甲烷菌生长。同时辅酶420活性检测也证实Nano–CuO发酵系统中消耗SCFAs的产甲烷菌活性较高。
分析结果发现,Nano–CuO和Nano–ZnO发酵系统中的蛋白质、多糖和SCFAs的产量显著低于碱性[17]、单过硫酸氢钾(PMS)[18]等发酵类型,这可能是因为发酵污泥性质不同,本实验发酵污泥为低有机质剩余污泥(MLVSS/MLSS ≤ 0.5),而对比实验发酵污泥为高有机质剩余污泥(MLVSS/MLSS ≥ 0.7)。同时,各发酵类型作用机制不同,碱性、PMS等发酵类型主要是通过强碱性或强氧化性离子对污泥进行直接破壁使有机质释放,而Nano–ZnO和Nano–CuO主要是依靠释放的Cu2+、Zn2+及部分带电物质作用于微生物蛋白质使微生物死亡自溶,因此Nano–CuO和Nano–ZnO发酵系统中蛋白质、多糖和SCFAs的产量相对较低。
2.2 NH4 +–N和PO4 3––P释放有机磷和有机氮是胞外聚合物(EPS)的组成部分,而且在厌氧微生物作用下能够将其转化为
由表3可知,同蛋白质、多糖相似,Nano–CuO发酵系统中,
蛋白酶和α–葡萄糖苷酶活性对于污泥水解具有至关重要的作用,蛋白酶和α–葡萄糖苷酶将蛋白质和多糖水解成小分子物质,如图2所示。由图2(a)、(b)可知,Nano–CuO和Nano–ZnO对蛋白酶和α–葡萄糖苷酶活性具有显著影响,其中,蛋白酶活性随着Nano–CuO和Nano–ZnO投加量的增加而增大,100 mg/L时蛋白酶活性分别为25.15和46.71 EU/mg VSS。研究发现蛋白酶活性随着Nano–ZnO浓度的增加而降低(1~150 mg/g TSS),这可能与Nano–ZnO的投加量有关[19]。α–葡萄糖苷酶活性随着Nano–CuO和Nano–ZnO投加量先增大后降低,最大值分别为0.0037 EU/mg VSS(10 mg /L,Nano–CuO)、0.0039 EU/mg VSS(1 mg /L,Nano–ZnO),可见,α–葡萄糖苷酶对于外界环境较蛋白酶更为敏感。Nano–ZnO发酵系统中蛋白酶和α–葡萄糖苷酶活性均高于Nano–CuO发酵系统,Nano–ZnO发酵系统中蛋白酶和α–葡萄糖苷酶水解蛋白质和多糖为酸化菌提供丰富的酸化底物,生成大量的SCFAs。蛋白酶活性显著高于α–葡萄糖苷酶活性,这是因为生物酶与其反应底物同时位于细胞体内,当反应底物从细胞内向细胞外转移时,生物酶也随之向外转移,因此,底物越丰富,相关生物酶活性越高。
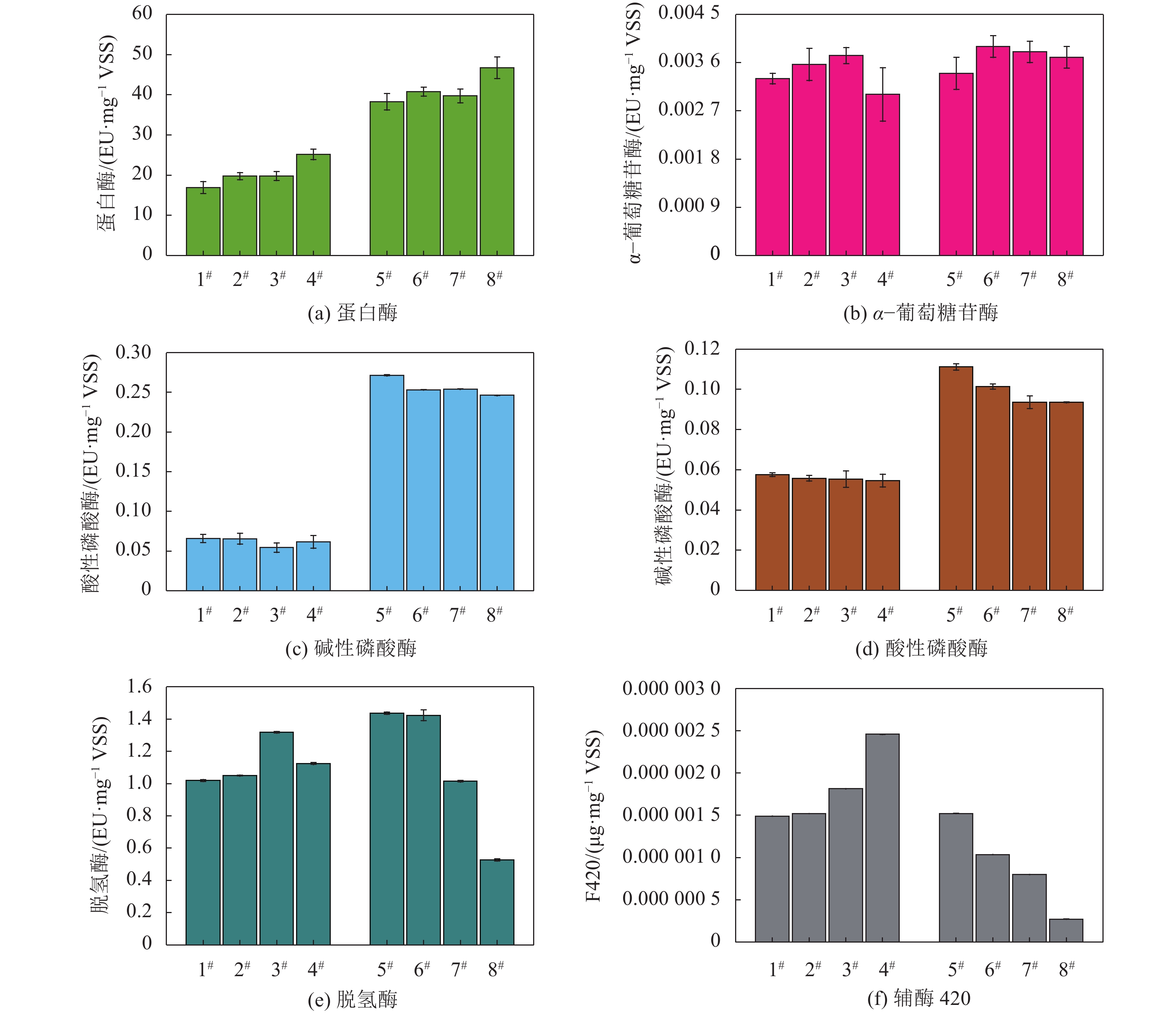 |
| 图2 Nano–CuO和Nano–ZnO对厌氧发酵系统生物酶活性的影响 Fig. 2 Effect of Nano–CuO and Nano–ZnO on bio-enzyme activity protease in anaerobic fermentation system |
2.3.2 碱性磷酸酶和酸性磷酸酶
微生物体内含有丰富的有机磷物质,污泥厌氧发酵过程中有机磷物质被磷酸酶(如碱性磷酸酶ALP、酸性磷酸酶ACP)作用于核苷酸、蛋白质等物质的磷酸基,ALP和ACP水解有机磷为无机磷并参与细胞内磷合成的新陈代谢[20]。分析图2(c)、(d)数据可知,Nano–CuO和Nano–ZnO对ALP和ACP具有显著的影响,其中,ALP和ACP均随着纳米颗粒浓度增加而降低,说明Nano–CuO和Nano–ZnO均能降低ALP和ACP活性。同时发现,Nano–ZnO发酵系统中ALP和ACP活性均大于Nano–CuO发酵系统,其中,ALP约为1.68~1.93倍,ACP约为3.86~4.68倍。可见,ALP和ACP对于Nano–ZnO耐受性高于Nano–CuO。
2.3.3 脱氢酶脱氢酶是一种重要的胞外酶,能够表征细胞膜破坏程度,在污泥厌氧发酵过程中具有至关重要的作用。图2(e)表明,脱氢酶活性随着Nano–CuO和Nano–ZnO浓度先增加后降低,其中,Nano–CuO发酵系统的脱氧酶活性为3#>4#>2#>1#,10 mg/L Nano–CuO发酵系统的脱氢酶最大为1.32 EU/mg VSS。Nano–ZnO发酵系统的脱氧酶浓度为6#>5#>7#>8#,1 mg/L Nano–ZnO发酵系统脱氢酶活性最大为1.42 EU/mg VSS。说明适当浓度的Nano–CuO和Nano–ZnO能够促进污泥厌氧发酵系统中的脱氢酶活性,这可能与纳米颗粒的聚集和络合作用有关[21]。
2.3.4 辅酶420SCFAs是污泥厌氧发酵末端产物,也是产甲烷菌主要作用基质,因此,污泥厌氧发酵系统中产甲烷菌活性是影响SCFAs积累的重要因素。辅酶420(F420)是衡量产甲烷菌活性的重要指标。分析图2(f)数据可知,辅酶420活性随着Nano–CuO浓度增加而增大,而随着Nano–ZnO浓度增加而降低。结果表明,0.1~100 mg /L(Nano–CuO)能够提高污泥发酵系统中产甲烷菌活性,但是,Nano–ZnO能够严重抑制产甲烷菌活性。这是因为Nano–ZnO释放的部分Zn2+能够抑制产甲烷菌新陈代谢活性,进而降低产甲烷菌活性[8]。Zhang等[16]也证实,Nano–ZnO能够显著抑制产甲烷菌活性。Chen等[8]研究证明,30~150 mg/g TSS Nano–ZnO能够引起18.3%~75.1%的甲烷产量降低。
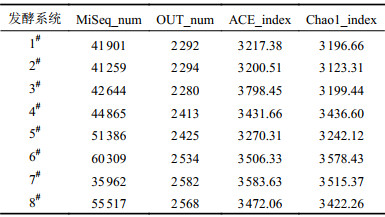
2.4 功能微生物种群分析 2.4.1 微生物群落变化为了更好地分析Nano–CuO和Nano–ZnO对污泥厌氧发酵系统微生物种群的影响,发酵末期将8个发酵系统发酵污泥进行高通量分析,如表4、5和图3所示。由表4可知,Nano–CuO发酵系统MiSeq序列和OUT分别为41901、2292(1#),41259、2294(2#),42644、2280(3#),44865、2413(4#),Nano–ZnO发酵系统MiSeq序列分别为51386、2425(5#),60309、2534(6#),55962、2582(7#),55517、2568(8#)。分析数据可知,Nano–ZnO发酵系统中MiSeq序列和OUT显著高于Nano–CuO发酵系统,如Chao1和ACE所示。
| 表4 不同发酵系统微生物检测数据 Tab. 4 Microbial test data of different fermentation systems |
 |
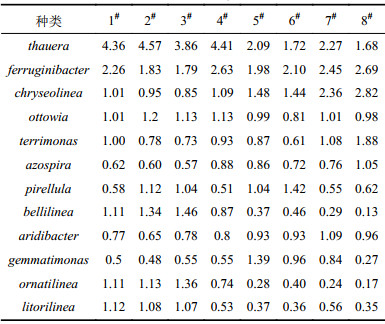
| 表5 Nano–CuO和 Nano–ZnO发酵系统中功能微生物种类 Tab. 5 Functional species of in Nano–CuO and Nano–ZnO levels fermentation systems |
 |
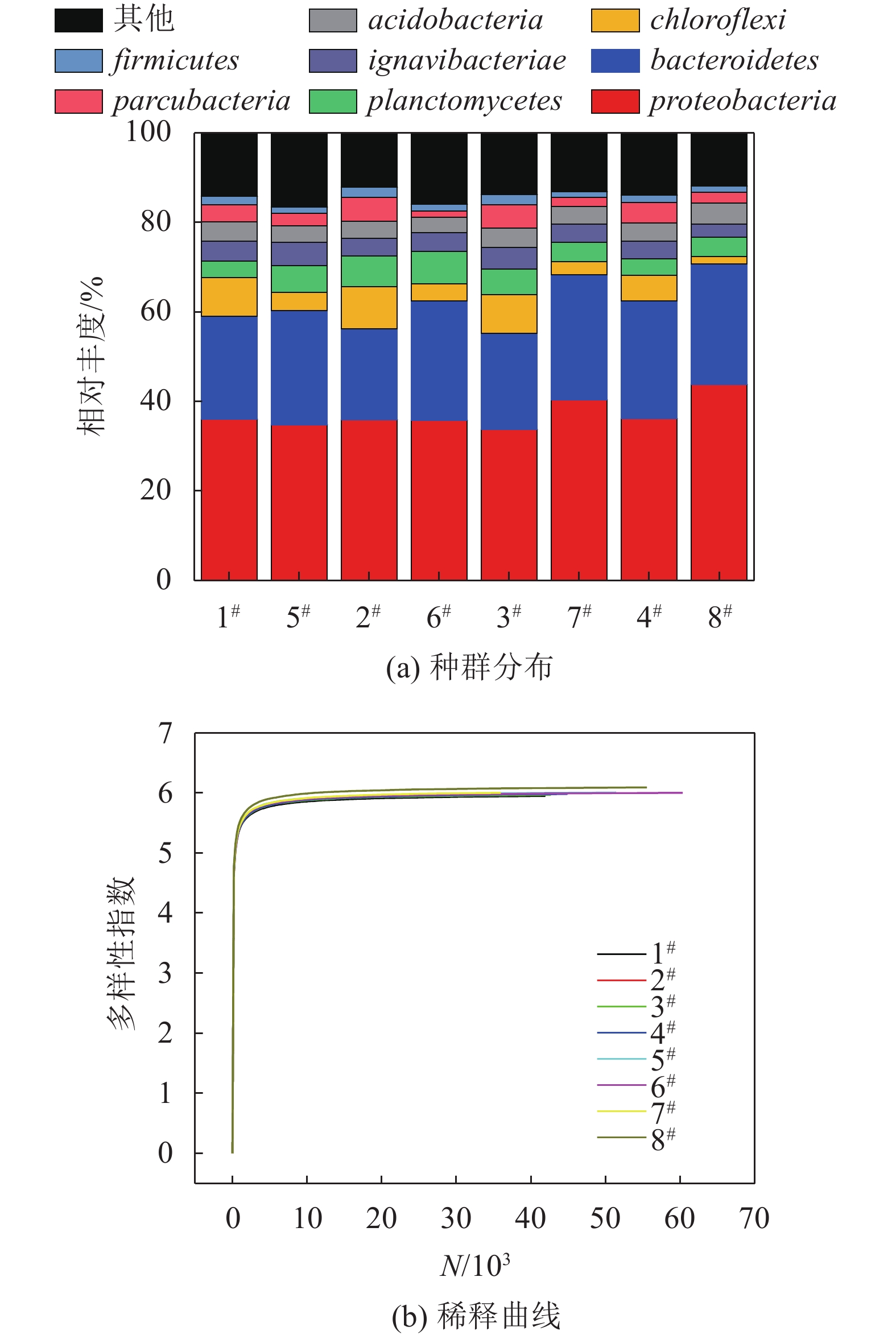 |
| 图3 Nano–ZnO和Nano–CuO发酵系统中微生物种群分布和稀释曲线 Fig. 3 Microbial population distribution and dilution curve of Nano–CuO and Nano–ZnO fermentation system |
同时图3(b)显示,Nano–CuO发酵系统中微生物多样性稀释曲线显著低于Nano–ZnO发酵系统,说明Nano–ZnO能够改善发酵系统微生物种群丰度。
2.4.2 功能微生物由图3(a)可知,8个发酵系统中分别检测到7个门类,分别为proteobacteria(Nano–CuO:35.99%、35.92%、33.77%、36.19%,Nano–ZnO:34.81%、35.79%、40.40%、43.81%)、bacteroidetes(Nano–CuO:23.10%、20.27%、21.49%、26.23%,Nano–ZnO:25.53%、26.66%、27.93%、26.92%)、chloroflexi(Nano–CuO:8.55%、9.43%、8.60%、5.81%,Nano–ZnO:4.01%、3.84%、2.95%、1.61%)、planctomycetes(Nano–CuO:3.70%、6.93%、5.75%、3.65%,Nano–ZnO:5.96%、7.22%、4.29%、4.35%)、acidobacteria(Nano–CuO:4.35%、3.81%、4.32%、4.04%,Nano–ZnO:3.77%、3.44%、3.92%、4.65%)、parcubacteria(Nano–CuO:3.76%、5.36%、5.13%、4.62%,Nano–ZnO:2.71%、1.46%、1.96%、2.46%)、ignavibacteriae(Nano–CuO:4.47%、3.88%、4.86%、3.99%,Nano–ZnO:5.20%、4.19%、4.07%、3.00%)。分析数据可知,Nano–ZnO发酵系统中的proteobacteria、planctomycetes和bacteroidetes含量显著高于Nano–CuO发酵系统,但是chloroflexi和parcubacteria含量低于Nano–CuO发酵系统,ignavibacteriae和planctomycetes含量相似。研究表明,proteobacteria在乙酸积累中具有重要作用[22]。由图3可见,Nano–ZnO发酵系统中proteobacteria含量显著高于Nano–CuO发酵系统,且随着Nano–ZnO浓度增加而增大。azospira、ottowia和hyphomicrobium功能菌属于proteobacteria,均能够分解乙酸、丙酸或者其他脂肪酸[23]。分析表5数据可知,Nano–ZnO和Nano–CuO发酵系统均发现azospira、ottowia菌群,同时Nano–ZnO发酵系统中azospira菌群含量显著高于Nano–CuO发酵系统,但是Nano–CuO发酵系统中ottowia含量高于Nano–ZnO发酵系统,这就可能造成Nano–ZnO和Nano–CuO发酵系统中SCFAs产量的差别。ferruginibacter对有机物具有较强的水解作用[24],其含量随着Nano–ZnO浓度的增加而增大,同时其含量显著高于Nano–CuO发酵系统,这与发酵系统中蛋白质和多糖含量相符(表1)。研究表明,terrimonas和chryseolinea含有丰富的碱性磷酸酶和α–葡萄糖苷酶,有助于淀粉和DNA等有机物的水解[25],这与Nano–CuO和Nano–ZnO发酵系统中碱性磷酸酶和多糖含量相符。aridibacter菌群富含碱性磷酸酶和酸性磷酸酶,同时能够水解蛋白质的有机物质[26]。thauera和nitrospira广泛分布于Nano–CuO发酵系统,说明Nano–CuO没能严重破坏微生物胞外聚合物结构,同时,该环境较为温和,有利于thauera的生长。通过功能菌群分析发现,Nano–ZnO发酵系统中较高浓度的水解菌群强化系统中SCFAs的积累。
3 结 论1)低有机质剩余污泥厌氧发酵系统中SCOD产量随着Nano–CuO和Nano–ZnO投加量的增加而增大;蛋白质和SCFAs产量随着Nano–ZnO浓度增加而增大,但是多糖产量随着Nano–CuO浓度的增加而降低。
2)Nano–CuO和Nano–ZnO对发酵系统中生物酶活性具有显著的影响,蛋白酶活性随着纳米颗粒投加量的增加而增大;α–葡萄糖苷酶和脱氢酶活性随着纳米颗粒投加量的增加而降低;
3)Nano–ZnO和Nano–CuO发酵系统均富集丰富的azospira、ottowia菌群;Nano–ZnO发酵系统含有大量的水解菌ferruginibacter和富含碱性磷酸酶、α–葡萄糖苷酶的terrimonas和chryseolinea。
本实验通过系统研究证实,与Nano–CuO相比,适当浓度的Nano–ZnO能够提高污泥水解性能,有利于污泥厌氧发酵系统中水解酸化菌生长,进而优化低有机质低浓度剩余污泥厌氧发酵产酸性能。因此,Nano–ZnO能够提高低有机质剩余污泥资源化处理。
| [1] |
Mortimer M,Kasemets K,Kahru A. Toxicity of ZnO and CuO nanoparticles to ciliated protozoa Tetrahymena thermophila[J]. Toxicology, 2010, 269(2/3): 182-189. DOI:10.1016/j.tox.2009.07.007 |
| [2] |
Gottschalk F,Sun Tianyin,Nowack B. Environmental concentrations of engineered nanomaterials:Review of modeling and analytical studies[J]. Environmental Pollution, 2013, 181: 287-300. DOI:10.1016/j.envpol.2013.06.003 |
| [3] |
Li Wei,ShiXianyang. Effects of ZnO nanoparticles on nitrogen removal performance and nitrifying bacteria abundance of activated sludge in SBR[J]. Chinese Journal of Environmental Engineering,, 2017, 11(8): 4549-4558. [李维,石先阳. 氧化锌纳米颗粒对SBR中活性污泥脱氮性能及硝化细菌丰度的影响[J]. 环境工程学报, 2017, 11(8): 4549-4558. DOI:10.12030/j.cjee.201606123] |
| [4] |
Ma Yongpeng,Wei Denghui,Zhang Xiaojing,et al. An innovative strategy for inducing Anammox from partial nitrification process in a membrane bioreactor[J]. Journal of Hazardous Materials, 2019, 379: 120809. DOI:10.1016/j.jhazmat.2019.120809 |
| [5] |
Zhang X,Zhou Y,Yu B,et al. Effect of copper oxide nanoparticles on the ammonia removal and microbial community of partial nitrification process[J]. Chemical Engineering Journal, 2017, 328: 152-158. DOI:10.1016/j.cej.2017.07.028 |
| [6] |
Zhang Zhengzhe,Xu Jiajia,Shi Zhijian,et al. Short-term impacts of Cu,CuO,ZnO and Ag nanoparticles (NPs) on anammox sludge:CuNPs make a difference[J]. Bioresource Technology, 2017, 235(19): 281-291. DOI:10.1016/j.biortech.2017.03.135 |
| [7] |
Adams L K,Lyou D Y,Alvarez P J J. Comparative eco-toxicity of nanoscale TiO2,SiO2,and ZnO water suspensions
[J]. Water Research, 2016, 40: 3527-3532. DOI:10.1016/j.watres.2006.08.004 |
| [8] |
Mu Hui,Chen Yinguang,Xiao Naidong. Effects of metal oxide nanoparticles (TiO2,Al2O3,SiO2 and ZnO) on waste activated sludge anaerobic digestion
[J]. Bioresource Technology, 2011, 102(22): 10305-10311. DOI:10.1016/j.biortech.2011.08.100 |
| [9] |
Li Xiaoming,Zhao Jianwei,Wang Dongbo,et al. An efficient and green pretreatment to stimulate short-chain fatty acids production from waste activated sludge anaerobic fermentation using free nitrous acid[J]. Chemosphere, 2016, 144: 160-167. DOI:10.1016/j.chemosphere.2015.08.076 |
| [10] |
Li Yanxia,Chen Tongbin,Luo Wei,et al. Contents of organic matter and major nutrients and the ecological effect related to land application of sewage sludge in China[J]. Acta Ecologica Sinica, 2003, 23(11): 2464-2474. [李艳霞,陈同斌,罗维,等. 中国城市污泥有机质及养分含量与土地利用[J]. 生态学报, 2003, 23(11): 2464-2474. DOI:10.3321/j.issn:1000-0933.2003.11.031] |
| [11] |
Liao Xiaocong,Li Huan. Biogas production from low-organic-content sludge using a high-solids anaerobic digester with improved agitation[J]. Applied Energy, 2015, 148: 252-259. DOI:10.1016/j.apenergy.2015.03.082 |
| [12] |
Sun Tong,Li Mingxing,Li Li,et al. Anaerobic co-digestion of kitchen dewatered greases and nutrient-deficient sludge[J]. Chinese Journal of Environmental Engineering, 2017, 11(6): 3899-3906. [孙通,李明星,李莉,等. 餐厨油脂与低热值污泥联合厌氧消化产气[J]. 环境工程学报, 2017, 11(6): 3899-3906. DOI:10.12030/j.cjee.201603118] |
| [13] |
Gilcreas F W. Standard methods for the examination of water and wastewater[J]. American Journalof Public Health and the Nation’s Health, 1995, 56(3): 387-388. DOI:10.1080/23267224.1919.10651076 |
| [14] |
Yuan H,Chen Y,Zhang H,et al. Improved bioproduction of short-chain fatty acids (SCFAs) from excess sludge under alkaline conditions[J]. Environmental Science &Technology, 2006, 40(3): 2025-2029. DOI:10.1021/es052252b |
| [15] |
Goel R,Mino T,Satoh H,et al. Enzyme activities under anaerobic and aerobic conditions in activated sludge sequencing batch reactor[J]. Water Research, 1998, 32: 2081-2088. DOI:10.1016/S0043-1354(97)00425-9 |
| [16] |
Zhang Lingling,He Xi,Zhang Zhaoxi,et al. Evaluating the influences of ZnO engineering nanomaterials on VFA accumulation in sludge anaerobic digestion[J]. Biochemical Engineering Journal, 2017, 125: 206-211. DOI:10.1016/j.bej.2017.05.008 |
| [17] |
Jin Baodan,Wang Shuying,Xing Liqun,et al. Long term effect of alkali types on waste activated sludge hydrolytic acidification and microbial community at low temperature[J]. Bioresource Technology, 2016, 200: 587-597. DOI:10.1016/j.biortech.2015.10.036 |
| [18] |
Jin Baodan,Niu Jintao,Dai Jingwen,et al. New insights into the enhancement of biochemical degradation potential from waste activated sludge with low organic content by potassium monopersulfate treatment[J]. Bioresource Technology, 2018, 265: 8-16. DOI:10.1016/j.biortech.2018.05.032 |
| [19] |
Mu Hui,Chen Yinguang. Long-term effect of ZnO nanoparticles on waste activated sludge anaerobic digestion[J]. Water Research, 2011, 45(17): 5612-5620. DOI:10.1016/j.watres.2011.08.022 |
| [20] |
van Ommen K F,Geesey G G. Localization and Identification of populations of phosphatase-active bacterial cells associated with activated sludge flocs[J]. Microbial Ecology, 1999, 38(3): 201-214. DOI:10.1007/s002489900170 |
| [21] |
Yang Yu,Zhang Chiqian,Hu Zhiqiang. Impact of metallic and metal oxide nanoparticles on wastewater treatment and anaerobic digestion[J]. Environmental Science(Processes & Impacts), 2012, 15(1): 39-48. DOI:10.1039/C2EM30655G |
| [22] |
Yuan Yue,Wang Shuying,Liu Ye,et al. Long-term effect of pH on short-chain fatty acids accumulation and microbial community in sludge fermentation systems[J]. Bioresource Technology, 2015, 197: 56-63. DOI:10.1016/j.biortech.2015.08.025 |
| [23] |
Hao Jiuxiao,Wang Hui. Volatile fatty acids productions by mesophilic and thermophilic sludge fermentation:Biological responses to fermentation temperature[J]. Bioresource Technology, 2015, 175: 367-373. DOI:10.1016/j.biortech.2014.10.106 |
| [24] |
Darchambeau F,Roland F,Crowe S A,et al.Denitrification,anammox and fixed nitrogen removal in the water column of a tropical great lake[C]//EGU General Assembly Conference,Vienna:EGU,2013.
|
| [25] |
Lim J H,Baek S H,Lee S T. Ferruginibacter alkalilentus gen.nov.,sp.nov.and Ferruginibacter lapsinanis sp.nov.,novel members of the family ‘chitinophagaceae’ in the phylum bacteroidetes,isolated from freshwater sediment
[J]. International Journal of Systematic & Evolutionary Microbiology, 2009, 59: 2394-2499. DOI:10.1099/ijs.0.009480-0 |
| [26] |
Wang Fengqing,Shen Qiyao,Chen Guanjun,et al. Mariniphaga sediminis sp.nov.,isolated from coastal sediment
[J]. International Journal of Systematic & Evolutionary Microbiology, 2015, 65(9): 2908-2912. DOI:10.1099/ijs.0.000354 |
 2021, Vol. 53
2021, Vol. 53

